|
ГЕТЕРОЛИТИЧЕСКИЕ РЕАКЦИИ (от греч. heteros-иной, другой и lysis-разложение,
распад), протекают с гетеролизом хим. связи, т.е. с таким ее разрывом,
при к-ром электронная пара, осуществляющая связь, остается у одного из
атомов и, как правило, образуются ионы:
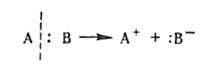
Иногда к гетеролитическим относят также р-ции, в к-рых образование новой
химической связи происходит в результате обобществления электронной пары
одного из реагентов.
Осуществлению Г. р. благоприятствует использование в кач-ве реагентов
сильных к-т или оснований, высокая диэлектрич. проницаемость среды. Гетеролиз
энергетически менее выгоден (на 300-650 кДж/моль), чем гомолиз (см. Гомолитические
реакции), однако в р-рах благодаря сольватации образующихся ионов Г.
р. протекают сравнительно легко.
В орг. химии Г. р. принято делить в зависимости от характера разрыва
связи С—X на нуклеофильные реакции (заместитель X уходит с электронной
парой и образуется карбкатион) и электрофильные реакции (электронная
пара остается у атома С и образуется карбанион). Механизм Г. р. иногда
может включать промежут. образование ионрадикалов, в этом случае говорят
о наличии стадии одно-электронного переноса.
Типичные Г. р.-распад молекул на ионы, рекомбинация ионов, мн. процессы
замещения, элиминирования и присоединения, в т.ч. такие промышленно важные,
как нитрование и сульфироваиие ароматич. соединений, присоединение галогенов
к олефинам в полярных р-рителях.
===
Исп. литература для статьи «ГЕТЕРОЛИТИЧЕСКИЕ РЕАКЦИИ»: Беккер Г., Введение в электронную теорию органических реакций,
пер. с нем., М., 1977.
Страница «ГЕТЕРОЛИТИЧЕСКИЕ РЕАКЦИИ» подготовлена по материалам химической энциклопедии.
|

