|
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, орг. соединения, молекулы
к-рых содержат циклы, включающие наряду с атомами углерода один или неск.
атомов др. элементов (гетероатомов). Наиб. значение имеют Т.е., в цикл
к-рых входят атомы N, О, S. К ним относятся мн, алкалоиды, витамины, антибиотики,
прир. пигменты; они входят в виде структурных фрагментов в молекулы нуклеиновых
к-т, белков и др. Г. с.-самый многочисленный класс орг. соед., включающий
ок. 2/3 всех известных прир. и синтетич. орг. веществ.
Номенклатура. Согласно правилам номенклатуры ИЮПАК, для важнейших
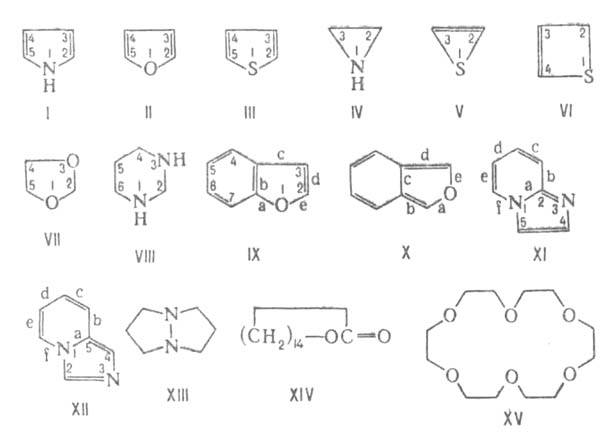
Г. с. сохраняются их тривиальные назв., напр. пиррол (ф-ла I), фуран
(II), тиофен (III). Систематич. назв. моноциклич. Т.е., содержащих
в цикле от 3 до 10 атомов, образуют путем сочетания приставок, обозначающих
гетероатомы (N-аза, О-окса, S-тиа, Р-фосфа и т. п.), с корнями, к-рые для
основных Г. с. приведены в таблице. Степень гидрогенизации ненасыщ. гетероцикла
отражается в назв. с помощью корней или приставок "дигидро" (присоединены
два атома водорода), "тетрагидро", "пергидро" и т.д. Примеры систематич.
назв.: азиридин (IV), тиирен (V), тает (VI), 1,3-диоксолан (VII), пергидропиримидин
(VIII).
При построении назв. в-в, молекулы к-рых состоят из конденсиров. циклов,
в кач-ве основы используют назв. "старшего" цикла. При этом учитывается,
что гетероцикл всегда старше карбоцикла, а среди гетероциклов предпочтение
отдается циклам с большим числом членов; при одинаковом размере двух циклов
старшинство определяется природой гетероатома (N > О > S). Связи в основном
цикле обозначаются строчными латинскими буквами: а-связи 1-2, b-связи
2-3 и т.д. Напр., изомеры бензофурана наз. бензо[b]фуран (IX) и
бензо[с]фуран (X). В случае конденсации с карбоциклом, имеющим неравноценные
положения, напр. с нафталиновым ядром, или с др. гетероциклом связи "младшего"
цикла нумеруются обычным образом, причем номера атомов "в месте конденсации"
указываются в порядке, соответствующем последовательности связей основного
цикла, напр. имидазо[1,2-а]пиридин (XI), имидазо[1,5-а]пиридин (XII).
Для Г. с, с 11 и более членами в цикле, мостиковых и нек-рых конденсиров.
систем используется "а"-номенклатура, по правилам к-рой первая составная
часть назв. обозначает гетероатом, а вторая-назв. углеводорода, к-рое м.
б. образовано, если считать, что в ф-ле Г. с. все гетероатомы заменены
на атомы С, группы СН или СН2, напр. 1,5-диазабицикло[3,3,0]октан
(Xill). Для названия Г.с. этого типа используют также традиционные назв.,
напр. пентадеканолид (XIV), 18-краун-6-эфир (XV).
КОРНИ, ИСПОЛЬЗУЕМЫЕ ПРИ СОСТАВЛЕНИИ НАЗВАНИЙ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
ПО НОМЕНКЛАТУРЕ ИЮПАК

* Содержат максимально возможное число некумулированных двойных связей.
** В скобках -корни назв. соответствующих насыш. соединений. Назв. насыщ.
гетероциклов с числом атомов более 5 имеют те же корни, Что и у ненасыщенных,
но с добавлением приставки "пергндро".
Химические свойства. Для 3- и 4-членных Г. с. характерна легкость
раскрытия напряженного цикла. 5- и 6-членные ненасыщ. гетероциклы (наиб.
многочисл. тип Г. с.), замкнутая сопряженная система связей к-рых включает
(4м + 2)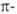 электронов,
обладают ароматич. характером (правило Хюккеля) и наз. гетероароматич.
соединениями. Для них, как и для бензоидных ароматич. соед., Наиб. характерны
р-ции замещения. При этом гетероатом играет роль "внутренней" ф-ции, определяющей
ориентацию, а также активирующее или дезактивирующее влияние на кольцо
к действию разл. реагентов. электронов,
обладают ароматич. характером (правило Хюккеля) и наз. гетероароматич.
соединениями. Для них, как и для бензоидных ароматич. соед., Наиб. характерны
р-ции замещения. При этом гетероатом играет роль "внутренней" ф-ции, определяющей
ориентацию, а также активирующее или дезактивирующее влияние на кольцо
к действию разл. реагентов.
Гетероароматич. соед. подразделяют на я-избыточные и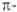 дефицитные.
К первым относят 5-членные Г. с. с одним гетероатомом, в к-рых секстет дефицитные.
К первым относят 5-членные Г. с. с одним гетероатомом, в к-рых секстет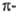 электронов
делокализован между пятью атомами цикла, что обусловливает их повыш. активность
по отношению к электроф. агентам. К электронов
делокализован между пятью атомами цикла, что обусловливает их повыш. активность
по отношению к электроф. агентам. К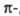 дефицитным
относят 6-членные гетероциклы с шестью дефицитным
относят 6-членные гетероциклы с шестью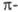 электронами,
к-рые распределяются, как и в случае бензола, между шестью атомами кольца,
но один или неск. из них - гетероатомы с большей, чем у углерода, электроотрицательностью.
Такие соед. напоминают по реакц. способности производные бензола, несущие
ориентанты II рода. Пятичленные гетероароматич. соед. с неск. гетероатомами
по формальному признаку можно было бы считать также электроноизбыточными,
однако наличие двух и более гетероатомов с их высокой электроотрицательностью,
а также способность превращ. в условиях электроф. замещения в соответствующие
катионы обусловливает то, что эти соед. по реакц. способности во многом
близки к электронодефицитным Г.с.; их иногда наз. электронами,
к-рые распределяются, как и в случае бензола, между шестью атомами кольца,
но один или неск. из них - гетероатомы с большей, чем у углерода, электроотрицательностью.
Такие соед. напоминают по реакц. способности производные бензола, несущие
ориентанты II рода. Пятичленные гетероароматич. соед. с неск. гетероатомами
по формальному признаку можно было бы считать также электроноизбыточными,
однако наличие двух и более гетероатомов с их высокой электроотрицательностью,
а также способность превращ. в условиях электроф. замещения в соответствующие
катионы обусловливает то, что эти соед. по реакц. способности во многом
близки к электронодефицитным Г.с.; их иногда наз.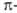 -амфотерными. -амфотерными.
Насыщенные, а также лишенные ароматичности ненасыщ. Г. с. с пятью и
более атомами в цикле напоминают по хим. св-вам соответствующие соед. с
открытой цепью-амины, эфиры, сульфиды и др.
===
Исп. литература для статьи «ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ»: Гетероциклические соединения, под ред. Р. Эльдерфилда,
пер. с англ., т. 1-8, М., 1953-69; Пакетт Л., Основы современной химии
гетероциклических соединений, пер. с англ., М., 1971; Джоуль Дж., Смит
Г., Основы химии гетероциклических соединений,пе,р. с англ., М., 1975;
Иванский В. И., Химия гетероциклических соединений, М., 1978; Наметкин
С. С., Гетероциклические соединения, М., 1981; Общая органическая химия,
под ред. Д. Бартона, У. Оллиса, пер. с англ., т. 8-9, М., 1985; Пожарский
А. Ф., Теоретические основы химии гетероциклов, М., 1985; The chemistry
of heterocyclic compounds, ed. by A. Weissberger, E. Teylor, v. 1-44, N.Y.-L.,
1950-85; Comprehensive heterocyclic chemistry, ed. by A.R. Katritzky, v.
1-8, N.Y.-[a.o.], 1984. Л.И. Беленъкш.
Страница «ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ» подготовлена по материалам химической энциклопедии.
|

