|
АЛЮМИНИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, содержат связь А1—С; общая ф-ла
RnАlХ3-n где R-орг. радикал; Х-Hal, H, OR, SR, NR2,
RCOO, CN и др.; п = 1-3. Различают симметричные, или полные, А.
с. (п = 3) и несимметричные, или смешанные.
А. с. чувствительны к влаге и О2 воздуха (соед. до С5
на воздухе самовоспламеняются). Поэтому все работы с А.с. выполняются в
атмосфере
сухого инертного газа, напр. азота или аргона. Alk3Al (см. табл.)
- бесцв. жидкости, Аг3А1 - твердые в-ва, растворимые в органических
растворителях.
Нек-рые А.с. - электрононенасыщенные соед., что обусловливает склонность
их молекул к ассоциации друг с другом. В образующихся димерах и тримерах
атомы А1 соединены через орг. радикалы трехцентровыми мостиковыми связями.
Известны также А.с. типа R2A1—A1R2. С донорами электронов,
напр. аминами и эфирами, А. с. образуют прочные аддукты состава 1 :1, с
анионными донорами MR или MX, где М - щелочной или щел.-зем. металл, -
солеобразные комплексы типа М [RnAlX4-n] (т. наз.
ат-комплексы).
СВОЙСГВА АЛЮМИНИЙОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
|
Соединение
|
Мол. м.
|
Т. пл., °С
|
Т. кип., °С/мм рт. ст.
|
Плотн. (25 °С), г/см3
|
|
Триметилалюминий (СН3)3А1
|
72,08
|
15
|
130
|
0,752 (при 20 °С)
|
|
Диметилалюминийхлорид (СН3)2А1С1
|
107,54
|
—
|
83-84/200
|
—
|
|
Триэтилалюминий (С2Н5)3А1
|
114,16
|
-52,5
|
136/100
|
0,875
|
|
Диэтилалюминийхлорид (С2Н5)2А1С1
|
120,56
|
-74
|
127/50
|
0,96
|
|
Этилалюминийдихлорид (С2Н,)А1С12
|
126,96
|
32
|
113/50
|
1,222
|
|
Тетраэтилалюминат натрия [(C2H5)4Al]Na
|
166,20
|
125
|
—
|
—
|
|
Трипропилалюминий (С3Н7)3А1
|
56,24
|
-84
|
110/10
|
0,820
|
|
Триизобутилалюминий (изо-С4Н9)3А1
|
198,33
|
-6
|
86/10
|
0,78
|
|
Диизобутилалюминийгидрид (изо-С4Н9)2А1Н
|
142,28
|
—
|
117/1
|
—
|
|
Диизобутилалюминийхлорид (мзо-С4Н9)2А1С1
|
176,06
|
-39
|
60/3
|
0,905
|
Основные р-ции А.с.: 1) бурное взаимод. с водой, к-тами, спиртами, аминами
и др. протонсодержащими соед. с выделением углеводородов, напр.: R3A1
+ nHOR' -> R3-nAl(OR')n + nRH; 2) окисление с образованием
алкоголятов: R3A1 + 1,5О2 -> (RO)3A1;
3) р-ция с СО2, приводящая к карбоновым к-там: R3A1
+
СО2 -> R2A1OC(O)R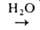 RCOOH; 4) взаимод. с галогенидами, оксидами и алкоголятами элементов более
электроотрицательными, чем А1 (В, Ga, Si, Sn, Pb и др.), с образованием
их алкилпроизводных, напр.: R3A1 + ЭНа1n -> RmЭHaln-m
+ А1На13 (п
RCOOH; 4) взаимод. с галогенидами, оксидами и алкоголятами элементов более
электроотрицательными, чем А1 (В, Ga, Si, Sn, Pb и др.), с образованием
их алкилпроизводных, напр.: R3A1 + ЭНа1n -> RmЭHaln-m
+ А1На13 (п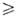 т;
п = 2, 3 или 4); 5) перераспределение орг. радикалов между симметричными
А. с. и галогенидами или алкоголятами Al, напр.: 2R3A1 + А1Х3
-> 3R2A1X; R3A1 + 2А1Х3 -> 3RA1X2;
6) р-ция с олефинами, в результате к-рой получают высшие А.с.: т;
п = 2, 3 или 4); 5) перераспределение орг. радикалов между симметричными
А. с. и галогенидами или алкоголятами Al, напр.: 2R3A1 + А1Х3
-> 3R2A1X; R3A1 + 2А1Х3 -> 3RA1X2;
6) р-ция с олефинами, в результате к-рой получают высшие А.с.: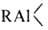 + nСН2=СН2 -> R—(—СН2СН2—)n—
+ nСН2=СН2 -> R—(—СН2СН2—)n—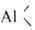 Способы получения А.с.: 1) взаимод. олефинов с А1 и Н2, напр.:
6СН2=СН2 + 2А1 + ЗН2 -> 2(С2Н5)3А1
(осн. пром. способ); 2) р-ция олефинов или ацетиленов с гидридами А1 (г
и д р о а л ю м и н и р о в а н и е), напр.: 3CH2=CHR + А1Н3
-> (RCH2CH2)3A1; НС
Способы получения А.с.: 1) взаимод. олефинов с А1 и Н2, напр.:
6СН2=СН2 + 2А1 + ЗН2 -> 2(С2Н5)3А1
(осн. пром. способ); 2) р-ция олефинов или ацетиленов с гидридами А1 (г
и д р о а л ю м и н и р о в а н и е), напр.: 3CH2=CHR + А1Н3
-> (RCH2CH2)3A1; НС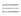 CR
+ R2A1H -> R2A1CH=CHR; 4CH2=CHR + МА1Н4
-> (RCH2CH2)4A1M (M=Na, Li); 3) переалкилирование
триизобутилалюминия олефинами: (изо-С4Н9)3А1
+ 3CH2=CHR -> (RCH2CH2)3A1
+ 3 изо-С4Н8. CR
+ R2A1H -> R2A1CH=CHR; 4CH2=CHR + МА1Н4
-> (RCH2CH2)4A1M (M=Na, Li); 3) переалкилирование
триизобутилалюминия олефинами: (изо-С4Н9)3А1
+ 3CH2=CHR -> (RCH2CH2)3A1
+ 3 изо-С4Н8.
Симметричные А. с. получают также р-цией галогенидов А1 с реактивами
Гриньяра или алкиллитием, действием диалкилртути на А1, дегалогенированием
несимметричных А.с. (напр, 3R2AlHal + 3Na -> 2R3A1
+ 3NaHal + А1). Несимметричные А. с. синтезируют взаимод. алкилгалогенидов
с А1, напр.: 3RHal + 2A1 -> R2AlHal + RAlHal2.
Элементный анализ А.с. заключается в сожжении навески в токе О2
с послед. определением С и Н гравиметрич. методом и одновременно А1 - по
кол-ву образовавшегося А12О3. Определение А1 возможно
также обычными методами неорг. анализа после гидролиза или алкоголиза А.
с. Состав образующихся при этом газообразных в-в устанавливают с помощью
ГЖХ.
А. с.-компоненты катализаторов Циглера - Натты, используемых в синтезе
полиолефинов и стереорегулярных диеновых каучуков, катализаторы стереоспецифич.
полимеризации полярных мономеров, напр. ацетальдегида, окисей олефинов,
капролактама, а также синтеза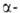 олефинов
нормального строения и др. На основе А. с. разработаны методы получения
высших жирных спиртов нормального строения высших жирных к-т, тетраэтилсвинца,
а также металлич. А1 высокой чистоты. Алюминийалкилы - восстановители при
получении карбонилов Мn, Сг, Мо и др., диалкилалюминийгидриды и комплексы
типа M[R2A1H2]-мягкие восстановители в орг. синтезе.
Мировое произ-во А. с. составляет десятки тыс. т/год (1982). См. также
Диэтилалюминийхлорид,
Триизобутилалюминий, Триэтилалюминий. олефинов
нормального строения и др. На основе А. с. разработаны методы получения
высших жирных спиртов нормального строения высших жирных к-т, тетраэтилсвинца,
а также металлич. А1 высокой чистоты. Алюминийалкилы - восстановители при
получении карбонилов Мn, Сг, Мо и др., диалкилалюминийгидриды и комплексы
типа M[R2A1H2]-мягкие восстановители в орг. синтезе.
Мировое произ-во А. с. составляет десятки тыс. т/год (1982). См. также
Диэтилалюминийхлорид,
Триизобутилалюминий, Триэтилалюминий.
===
Исп. литература для статьи «АЛЮМИНИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ»: Несмеянов А. Н., Соколик Р.А., в кн.: Методы элементоорганической
химии. Бор, алюминий, галлий, индий, таллий, под ред. А.Н. Несмеянова и
К.А. Кочешкова, М., 1964, с. 283-385; Комплексы металлоорганических, гибридных
и галоидных соединений алюминия, М., 1970; Корнеев Н.Н., Химия и технология
алюминийорганических соединений, М., 1979; Толстиков Г.А., Юрьев В. П.,
Алюминийорганический синтез, М., 1979. В. В. Гаврилето.
Страница «АЛЮМИНИЙОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ» подготовлена по материалам химической энциклопедии.
|

