|
АЛЮМОГИДРИДЫ (тетрагидридоалюминаты, аланаты), комплексные гидриды,
содержащие ион [А1Н4]-. Легко окисляются О2,
энергично взаимод. с водой, р-рами к-т и щелочей, выделяя Н2.
С аммиаком, галогенидами металлов и неметаллов образуют сложные комплексы.
Восстанавливают орг. соед. по кратным связям углерода с др. элементами,
не затрагивая связи С=С. Используют А. как селективные восстановители и
источники Н2, для получения гидридов элементов, при нанесении
металлических покрытий.
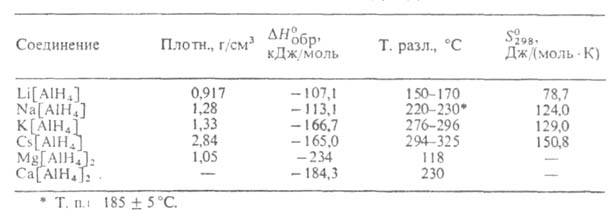
А. щелочных и щел.-зем. металлов (см. табл.) - бесцв. кристаллы, разлагающиеся
при нагр. (алюмогидрид Be разлагается в эфире уже при - 10°С). Они раств.
в ТГФ, диглиме и моноглиме, алюмогидриды Li и Mg- также в эфире. С орг.
р-рителями (напр., с эфиром) образуют сольваты. Особенно прочны сольваты
алюмогидридов Mg и Be, полное разложение к-рых сопровождается распадом
самих А. Свободные А. выделяют из р-ров в эфире и ТГФ путем отгонки р-рителя,
из р-ров в ТГФ и диглиме высаливанием эфиром или толуолом. наиб. распространенные
способы получения: взаимод. гидрида металла с А1На13 в полярном
орг. р-рителе; прямой синтез из металла, А1 и Н2 при 100-200°С
и повышенном давлении Н2 в сольватирующих р-рителях или в среде
углеводородов в" присут. катализатора (алюминийорг. соед.); обменные р-ции
галогенидов или борогидридов металлов с алюмогидридом Li или Na; по р-ции:
Li[AlH4] + М -> М [А1Н4] + Li, где М = Na, К, Rb,
Cs.
СВОЙСТВА АЛЮМОГИДРИДОВ
А. непереходных металлов групп III и IV и переходных металлов крайне
неустойчивы. Их обычно получают взаимод. Li[AlH4] с галогенидами
металлов в эфире при т-рах от —120 до — 80°С. При повышении т-ры эти А.
разлагаются с выделением Н2, (А1Н3)n и
металла.
А. четвертичных аммониевых оснований имеют общую ф-лу R4N[A1H4].
Если R - низший алкил, то А - кристаллы, если высший, А. - вязкие жидкости,
более стойкие к окислению и гидролизу, чем производные низших оснований.
Получают эти соединения обменной реакцией Li[AlH4] с R4NHal.
К А. относят также гидриды, содержащие ион [А1Н6]3-(напр.,
Na3[AlH6] с плотн. 1,48 г/см3 и т. разл.
260°С), сложные комплексы, образуемые гидридоалюминатами щелочных и щел.-зем.
металлов, напр. р-римые в эфире Li2[Mg(AlH4)4],
Li[Mg(AlH4)3Cl].
Для синтеза витаминов, спиртов, оптически активных соед. используют
А. общей ф-лы М[А1НnХ4-n], где Х-алкокси и др. О
три-трет-бутоксиалюмогидриде Li см. Лития алюмогидрид.
===
Исп. литература для статьи «АЛЮМОГИДРИДЫ»: Комплексы металлоорганических, гидридных и галоидных соединений
алюминия, М., 1970; Wiberg E., Amberger E., Hydrides of the elements main
groups I-IV, Amst.-L-N. Y., 1971. См. также лит. при ст. Борогидриды
металлов. А.И.Горбунов, П.А. Стороженко.
Страница «АЛЮМОГИДРИДЫ» подготовлена по материалам химической энциклопедии.
|

