| СОДЕРЖАНИЕ: |
НАУКА и ТЕХНОЛОГИИ |
ТЕНДЕНЦИИ РЫНКА |
ЭКОЛОГИЯ |
СОТРУДНИЧЕСТВО |
СОБЫТИЯ ОТРАСЛИ |
|
|
|
|
СЛОВАРЬ ТЕРМИНОВ
|
|
|
|
|
Алфавитный указатель:
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Щ
Э
Ю
Я
|
КАРБОНАТЫ НЕОРГАНИЧЕСКИЕ (от лат. carbo, род. падеж carbonis - уголь), соли угольной к-ты. Существуют средние карбонаты (К.) с анионом СО32- и кислые, или гидрокарбонаты (устар. бикарбонаты), с анионом HCO3-. К. - кристаллич. в-ва. Большинство средних солей металлов в степени окисления +2 кристаллизуется в гексагoн. решетке типа кальцита или ромбич. типа арагонита.
Из средних К. в воде раств. только соли щелочных металлов, аммония и Тl(I). В результате значит. гидролиза
их р-ры имеют щелочную р-цию. наиб. трудно раств. К. металлов в степени окисления +2 (см. табл.). Напротив, все гидрокарбонаты хорошо раств. в воде. При обменных р-циях в водных р-рах между солями металлов и Na2CO3 осадки средних К. образуются в тех случаях, когда их р-римость значительно меньше, чем соответствующих гидроксидов. Это имеет место для Са, Sr и их аналогов, лантаноидов, Ag(I), Mn(II), Pb(II) и Cd(II).
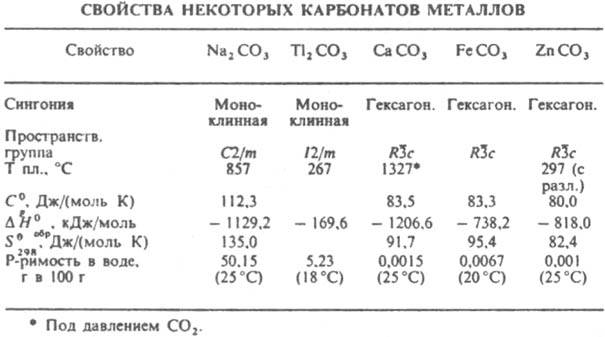
Остальные катионы при взаимод. с растворенными К. в результате гидролиза могут давать не средние, а основные К. или даже гидроксиды. Средние К., содержащие многозарядные катионы, иногда удается осадить из водных р-ров в присут. большого избытка СО2.
Хим. св-ва К. обусловлены их принадлежностью к классу неорг. солей слабых к-т. Характерные особенности К. связаны с их плохой р-римостью, а также термич. нестойкостью как самих К., так и Н2СО3. Эти св-ва используются при анализе К., основанном либо на их разложении сильными к-тами и количеств. поглощении выделяющегося при этом СО2 р-ром щелочи, либо на осаждении иона СО32- из р-ра в виде ВаСО3. При действии избытка СО2 на осадок среднего К. в р-ре образуется гидрокарбонат, напр.: СаСО3 + Н2О + СО2 : Са(НСО3)2. Присутствие гидрокарбонатов в прир. воде обусловливает ее временную жесткость (см. Жесткость воды). Гидрокарбонаты при легком нагр. уже при низких т-рах вновь превращаются в средние К., к-рые при нагр. разлагаются до оксида и СО2. Чем активнее металл, тем выше т-ра разложения его К. Так, Na2CO3 плавится без разложения при 857 °С, а для карбонатов Са, Mg и Аl равновесные давления разложения достигают 0,1 МПа при т-рах соотв. 820, 350 и 100 °С.
К. весьма широко распространены в природе, что обусловлено участием СО2 и Н2О в процессах минералообразования. К. играют большую роль в глобальных равновесиях между газообразным СО2 в атмосфере, растворенным СО2 и ионами HCO3- и СО32- в гидросфере и твердыми солями в литосфере. Важнейшие минералы - кальцит СаСО3, магнезит MgCO3, сидерит FeCO3, смитсонит ZnCO3 и нек-рые др. (см. Карбонаты природные). Известняк состоит в осн. из кальцита или кальцитовых скелетных остатков организмов, редко из арагонита. Известны также прир. гидратированные К. щелочных металлов и Mg (напр., MgCO3.3H2O, Na2CO3.10H2O), двойные К. [напр., доломит CaMg(CO3)2, трона Na2CO3.NaHCO3.2H2O] и основные [малахит CuCO3.Cu(OH)2, гидроцеруссит 2РbСО3.Рb(ОН)2].
Hаиб. важны калия карбонат, кальция карбонат и натрия карбонат. Мн. прир. К. весьма ценные металлич. руды (напр., карбонаты Zn, Fe, Mn, Pb, Cu). Гидрокарбонаты выполняют важную физиол. роль, являясь буферными в-вами, регулирующими постоянство рН крови.
П. М. Чукуров.
===
Исп. литература для статьи «КАРБОНАТЫ НЕОРГАНИЧЕСКИЕ»: нет данных
Страница «КАРБОНАТЫ НЕОРГАНИЧЕСКИЕ» подготовлена по материалам химической энциклопедии.
|
|
|
|

|
|
Куплю
19.04.2011 Белорусские рубли в Москве Москва 18.04.2011 Индустриальные масла: И-8А, ИГНЕ-68, ИГНЕ-32, ИС-20, ИГС-68,И-5А, И-40А, И-50А, ИЛС-5, ИЛС-10, ИЛС-220(Мо), ИГП, ИТД Москва 04.04.2011 Куплю Биг-Бэги, МКР на переработку. Москва |
Продам
19.04.2011 Продаем скипидар Нижний Новгород 19.04.2011 Продаем растворители Нижний Новгород 19.04.2011 Продаем бочки новые и б/у. Нижний Новгород |
|
|

