| СОДЕРЖАНИЕ: |
НАУКА и ТЕХНОЛОГИИ |
ТЕНДЕНЦИИ РЫНКА |
ЭКОЛОГИЯ |
СОТРУДНИЧЕСТВО |
СОБЫТИЯ ОТРАСЛИ |
|
|
|
|
СЛОВАРЬ ТЕРМИНОВ
|
|
|
|
|
Алфавитный указатель:
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Щ
Э
Ю
Я
|
КОНКУРИРУЮЩИХ РЕАКЦИЙ МЕТОД в химической кинетике, основан на том, что одна и та же активная частица (атом, своб. радикал, ион) может одновременно участвовать в неск. р-циях с образованием разл. продуктов. Условия подбираются такими, при к-рых параллельные р-ции протекают с соизмеримыми скоростями. Из соотношения скоростей этих р-ций (или концентраций образовавшихся продуктов) вычисляют отношения констант
скорости р-ций исследуемой частицы с соответствующими реагентами. К. р. м. применяют для изучения гл. обр. радикальных и ионных р-ций; он позволяет вычислять абс. значения констант скорости быстрых р-ций, оценивать реакц. способность разл. атомных групп в молекуле, в сочетании с методом изотопных индикаторов определять кинетический изотопный эффект.
Конкурирующие р-ции м. б. разного типа. В частности, это м.б. конкуренция между моно- и бимолекулярной р-циями. Напр., при термич. распаде трет-бутилпероксида в присут. углеводорода RH протекают р-ции:
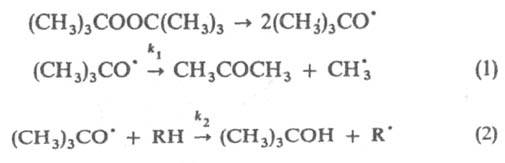
Образующиеся радикалы 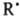 , , 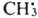 и и 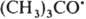 рекомбинируют. Отношение скоростей р-ций (2) и (1) v2/v1=k2[RH]/kl. Если в системе избыток RH, то v2/vl=[(СН3)3СОН]/[СН3СОСН3] и можно определить k2/k1=[(CH3)3COH]/[СН3СОСН3] [RH]. Поскольку известна при т-ре Т k1=3,2.1013ехр[(-69 кДж/моль-1)/RT] с-1 (газовая фаза), метод позволяет определить k2 (R-газовая постоянная).
При изучении радикальных р-ций часто используют конкуренцию между рекомбинацией радикалов и их взаимод. с молекулами. Напр., при изучении р-ций СН3 проводят фотолиз паров ацетона в присут. углеводорода RH, что вызывает протекание р-ций: рекомбинируют. Отношение скоростей р-ций (2) и (1) v2/v1=k2[RH]/kl. Если в системе избыток RH, то v2/vl=[(СН3)3СОН]/[СН3СОСН3] и можно определить k2/k1=[(CH3)3COH]/[СН3СОСН3] [RH]. Поскольку известна при т-ре Т k1=3,2.1013ехр[(-69 кДж/моль-1)/RT] с-1 (газовая фаза), метод позволяет определить k2 (R-газовая постоянная).
При изучении радикальных р-ций часто используют конкуренцию между рекомбинацией радикалов и их взаимод. с молекулами. Напр., при изучении р-ций СН3 проводят фотолиз паров ацетона в присут. углеводорода RH, что вызывает протекание р-ций:
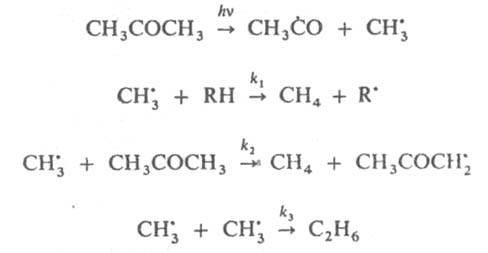
Измеряются скорости образования метана 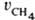 и этана и этана 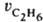 ; отношение ; отношение
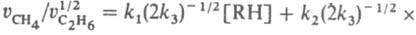
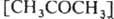 , ,
что позволяет вычислить k1 и k2 при известной k3=2.1010 л/моль.с (газовая фаза, давление выше 10 кПа). Этим методом измерены константы скорости гомолитич. распада для неск. сотен соединений.
Если в молекуле имеется неск. реакц. центров, анализ образующихся изомеров позволяет определить относит, реакц. способность каждого из этих центров. Напр., при нитровании толуола азотной к-той образуются о-, м- и n-нитротолуолы:
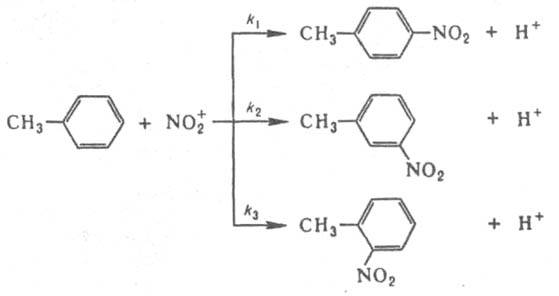
Соотношение между кол-вами о-, м- и n-нитротолуолов равно 2k3:2k2:k1.
===
Исп. литература для статьи «КОНКУРИРУЮЩИХ РЕАКЦИЙ МЕТОД»: Кондратьев В. Н., Определение констант скорости газофазных реакций, М., 1971; Денисов Е. Т., Кинетика гомогенных химических реакций, М.. 1978. Е. Т. Денисов.
Страница «КОНКУРИРУЮЩИХ РЕАКЦИЙ МЕТОД» подготовлена по материалам химической энциклопедии.
|
|
|
|

|
|
Куплю
19.04.2011 Белорусские рубли в Москве Москва 18.04.2011 Индустриальные масла: И-8А, ИГНЕ-68, ИГНЕ-32, ИС-20, ИГС-68,И-5А, И-40А, И-50А, ИЛС-5, ИЛС-10, ИЛС-220(Мо), ИГП, ИТД Москва 04.04.2011 Куплю Биг-Бэги, МКР на переработку. Москва |
Продам
19.04.2011 Продаем скипидар Нижний Новгород 19.04.2011 Продаем растворители Нижний Новгород 19.04.2011 Продаем бочки новые и б/у. Нижний Новгород |
|
|

