| СОДЕРЖАНИЕ: |
НАУКА и ТЕХНОЛОГИИ |
ТЕНДЕНЦИИ РЫНКА |
ЭКОЛОГИЯ |
СОТРУДНИЧЕСТВО |
СОБЫТИЯ ОТРАСЛИ |
|
|
|
|
СЛОВАРЬ ТЕРМИНОВ
|
|
|
|
|
Алфавитный указатель:
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Щ
Э
Ю
Я
|
КРАТНЫЕ СВЯЗИ, хим. связи двухцентрового типа, к-рые в отличие от простой связи образованы более чем одной парой электронов. По числу пар электронов, образующих К. с., различают двойные, тройные и четверные связи.
В приближении молекулярных орбиталей методов К. с. сопоставляются с мол. орбиталями, к-рые по св-вам симметрии делят на s-, p- и d-орбитали. p-Орбитали антисимметричны относительно плоскости, проходящей через связь. В многоатомных молекулах эта плоскость является общей для всей молекулы или для мол. фрагмента, включающего эту связь. d-Орбитали антисимметричны относительно двух взаимно перпендикулярных плоскостей, проходящих через связь. При образовании К. с. возникает, как правило, одна
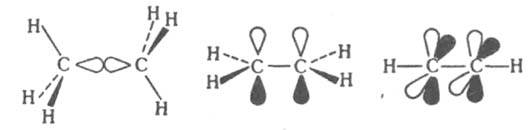
(или более) s-орбиталь и обязательно хотя бы одна p- или d-орбиталь. По этой причине составляющие К. с., определяемые p- или d-орбиталями, наз. соотв. p- или d-связями. Атомы непереходных элементов в молекулах и ионах м. б. связаны простой, двойной и тройной связями. Образование простой d-связи С—С в молекуле этана соотносят с перекрыванием двух sp3-гибридных орбиталей атомов углерода. В молекуле этилена кроме s-связи С—С присутствует одна, а в молекуле ацетилена с тройной связью - две p-связи:
Четверная связь (и м. б. связи более высокой кратности) характерна только для переходных металлов. d-Перскрываниe ведет к образованию четверных связей в солях октагалогеиодиренат-аниона Re2Hal82-, карбоксилатах молибдена и вольфрама M(OOCR)4, внутрикомплексных соед. хрома и ванадия М2А2, где А - 2,6-диметоксифенил.
Энергетич. вклады, приходящиеся на связи разл. типов, неравноценны. Обычно энергия p-связи составляет в среднем около 80% энергии s-связи, а вклад d-связи оценивается, напр., в солях октахлородирснат-аниона всего в 14% от полной энергии связи. Чем выше кратность связи, тем больше ее прочность (энергия диссоциации), короче межатомное расстояние и больше силовая постоянная связи (см. табл.).

Две или больше К. с. могут образовывать в хим. соединении системы кумулированных и сопряженных связей. В первом случае две двойные связи примыкают к одному и тому же атому как, напр., в аллене Н2С=С=СН2; во втором - двойные или (и) тройные связи разделены одной простой, как, напр., в 1,3-бутадиене Н2С=СН—СН=СН2 или акрилонитриле 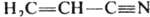 . В сопряженных системах кратность связи не м. б. определена целым числом. Мерой кратности связи (заселенности ее электронами) служит дробная величина порядка связи, расчет к-рой осуществляется обычно при помощи методов квантовой химии. . В сопряженных системах кратность связи не м. б. определена целым числом. Мерой кратности связи (заселенности ее электронами) служит дробная величина порядка связи, расчет к-рой осуществляется обычно при помощи методов квантовой химии.
===
Исп. литература для статьи «КРАТНЫЕ СВЯЗИ»: Гиллеспи Р., Геометрия молекул, пер. с англ., М., 1975; Коттон Ф. А., Уолтон Р., Кратные связи металл — металл, пер. с англ., М., 1985.
В. И. Минкин.
Страница «КРАТНЫЕ СВЯЗИ» подготовлена по материалам химической энциклопедии.
|
|
|
|

|
|
Куплю
19.04.2011 Белорусские рубли в Москве Москва 18.04.2011 Индустриальные масла: И-8А, ИГНЕ-68, ИГНЕ-32, ИС-20, ИГС-68,И-5А, И-40А, И-50А, ИЛС-5, ИЛС-10, ИЛС-220(Мо), ИГП, ИТД Москва 04.04.2011 Куплю Биг-Бэги, МКР на переработку. Москва |
Продам
19.04.2011 Продаем скипидар Нижний Новгород 19.04.2011 Продаем растворители Нижний Новгород 19.04.2011 Продаем бочки новые и б/у. Нижний Новгород |
|
|

