|
АММОНИЯ НИТРАТ (аммиачная селитра) NH4NO3,
бесцв. гигроскопичные кристаллы; т. пл. 169,6°С, т. кип. 235 °С. Сведения
о кристаллич. модификациях приведены в таблице.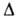 Н°
полиморфных
переходов IV Н°
полиморфных
переходов IV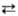 Ш
1,7 кДж/моль, III Ш
1,7 кДж/моль, III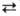 П
1,3 кДж/моль. При переходах II -> III, IV -> III и IV -> V объем элементарной
ячейки увеличивается. П
1,3 кДж/моль. При переходах II -> III, IV -> III и IV -> V объем элементарной
ячейки увеличивается.
СВОЙСТВА КРИСТАЛЛИЧЕСКИХ МОДИФИКАЦИЙ NH4NO3
|
Модификация
|
Кристаллич. решетка
|
Область существования,
|
Параметры решетки, нм
|
|
а
|
b
|
с
|
|
I
|
Кубич.
|
125,8-169,6
|
0,441
|
|
|
|
II
|
Тетрагон.
|
84,2-125,8
|
0,576
|
_
|
0,502
|
|
III
|
Ромбич.
|
32,2-84,2
|
0,718
|
0,771
|
0,583
|
|
IV
|
Ромбич.
|
от 32,2 до -16,9
|
0,494
|
0,544
|
0,575
|
|
V
|
Тетрагон.
|
Ниже -16,9
|
0,572
|
—
|
1,600
|
Для модификации IV: плотн. 1,725 г/см3; Сp° 139,4
ДжДмоль*К); Н°пл5,86
к Дж/моль, Н°пл5,86
к Дж/моль,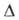 Нообр
-365,7 кДж/моль, Нообр
-365,7 кДж/моль,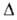 СобР -184 кДж/моль; S°298 151,1 Дж/(моль*К).
Для жидкого А.н. плотн. 1,436 г/см3 (170°С), 1,414 г/см3
(220°С);
СобР -184 кДж/моль; S°298 151,1 Дж/(моль*К).
Для жидкого А.н. плотн. 1,436 г/см3 (170°С), 1,414 г/см3
(220°С);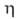 5,71 мПа*с (170°С), 3,23 мПа*с (220°С);
5,71 мПа*с (170°С), 3,23 мПа*с (220°С);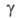 98,8 мН/м2 (179°С), 98,4 мН/м2 (187°С);
98,8 мН/м2 (179°С), 98,4 мН/м2 (187°С);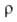 2,5 Ом*см (175°С). Ур-ния температурной зависимости давления пара: Ig p
(мм рт. ст.) = 10,708 - 4670/Т (349-438 К), I gp (мм рт. ст.) = 9,981 -
4360/Т (373-513 К). Р-римость А.н. (г в 100 г р-рителя): в воде -119 (0°С),
212 (25°С), 346 (50°С); жидком NH3-391 (25 °С). Раств. также
в метаноле, этаноле, пиридине. При 200-270°С разлагается: NH4NO3
-> N2O+ 2Н2О + 36,8 кДж/моль. Выше 270°С или при
воздействии удара может разлагаться со взрывом:
2,5 Ом*см (175°С). Ур-ния температурной зависимости давления пара: Ig p
(мм рт. ст.) = 10,708 - 4670/Т (349-438 К), I gp (мм рт. ст.) = 9,981 -
4360/Т (373-513 К). Р-римость А.н. (г в 100 г р-рителя): в воде -119 (0°С),
212 (25°С), 346 (50°С); жидком NH3-391 (25 °С). Раств. также
в метаноле, этаноле, пиридине. При 200-270°С разлагается: NH4NO3
-> N2O+ 2Н2О + 36,8 кДж/моль. Выше 270°С или при
воздействии удара может разлагаться со взрывом:
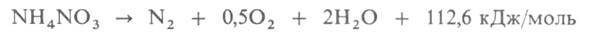
А.н. обычно получают нейтрализацией 60%-ной HNO3 газообразным
NH3 с использованием теплоты р-ции (145 кДж/моль) для упаривания
р-ра NH4NO3. Образующийся А.н. гранулируют. Для получения
прочных гранул, обеспечивающих возможность бестарных перевозок, и повышения
срока хранения в А.н. вводят (NH4)2SO4,
Mg(NO3)2 или смесь (NH4)2SO4
с NH4H2PO4 (обычно не более 0,5% по массе).
Мощность агрегатов по произ-ву А. н. до 450-520 тыс.т/год.
А. н. - азотное удобрение. Его применяют также в произ-ве ВВ (напр.,
аммонитов, гранулитов), как реагент для растворения циркониевых оболочек
твэлов при регенерации облученного ядерного топлива. Мировое произ-во 14
млн. т/год в пересчете на азот (1980). А.н. впервые был получен И.Р. Глаубером
в 1659.
===
Исп. литература для статьи «АММОНИЯ НИТРАТ»: Технология аммиачной селитры, под ред. В. М. Олевского,
М., 1978; Олевский В. М., Ферд М. Л., "Ж. Всес. хим. о-ва им. Д.И.Менделеева",
1983, т. 28, № 4, с. 27-39. В.М. Олевский.
Страница «АММОНИЯ НИТРАТ» подготовлена по материалам химической энциклопедии.
|

