| СОДЕРЖАНИЕ: |
НАУКА и ТЕХНОЛОГИИ |
ТЕНДЕНЦИИ РЫНКА |
ЭКОЛОГИЯ |
СОТРУДНИЧЕСТВО |
СОБЫТИЯ ОТРАСЛИ |
|
|
|
|
СЛОВАРЬ ТЕРМИНОВ
|
|
|
|
|
Алфавитный указатель:
А
Б
В
Г
Д
Е
Ж
З
И
К
Л
М
Н
О
П
Р
С
Т
У
Ф
Х
Ц
Ч
Ш
Щ
Э
Ю
Я
|
МАГНИЯ КАРБОНАТ MgCO3, бесцв. кристаллы с гексагон. решеткой (а = 0,4633 нм, с = 1,5016 нм, z = 6,
пространств. группа 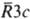 ); т. пл. 990 °С (с разл.); плотн. 3,0 г/см3; С0р 76,11 Дж/(моль.К); DH0пл 59 кДж/моль, DH0обр -1096 кДж/моль; S0298 65,09 Дж/(моль.К); твердость по Моосу 3,5-4,5. Начинает разлагаться до MgO при 350 °С, давление диссоциации 0,1 МПа достигается при ~650°С. Р-римость М.к. в воде в отсутствие СО2 ~ 0,5 мг/л, под давлением СО2 она сильно возрастает. В водном р-ре М.к. сильно гидролизуется, поэтому при действии р-ров карбонатов металлов на р-ры солей Mg в р-ре образуются основные карбонаты состава xMgCO3.yMg(OH)2.zH2O, a MgCO3 м. б. получен только при действии КНСО3 в присут. большого избытка СО2 в р-ре. Безводный М.к. встречается в природе в виде минерала магнезита.
В системе MgCO3-H2O кристаллизуются пента-, три- и моногидраты М.к. Пентагидрат MgCO3.5H2O (минерал ландсфордит) - бесцв. кристаллы с моноклинной решеткой (а = 1,2369 нм, b = 0,7520 нм, с = 0,7315 нм, b = 99,6°, z = 4, пространств. группа P21/m); плотн. 1,72 г/см3; DH0обр -2566,9 кДж/моль, DG0обр -2199,9 кДж/моль; р-римость 0,18 г в 100 г Н2О при 20°С. Тригидрат MgCO3.3H2O (минерал несквегонит) - бесцв. кристаллы с моноклинной решеткой (а = 1,2112 нм, b = 0,5365 нм, с = 0,7697 нм, b = 90,7°, z = 4, пространств. группа Р21/т); плотн. 1,84 г/см3; DH0обр -1977,0 кДж/моль; р-римость 0,11 г в 100 г Н2О при 20 °С. При нагр. пентагидрат переходит в тригидрат, а при 60-80°С образуется основной карбонат состава 4MgCO3.Mg(OH)2.5H2O, к-рый выше 200 °С начинает разлагаться до MgO.
При насыщении водной суспензии М.к. СО2 происходит растворение М.к. и образуется гидрокарбонат Mg(HCO3)2, существующий только в р-ре. При взаимод. MgCO3 с карбонатами щелочных и щел.-зем. металлов образуются плохо р-римые двойные карбонаты, напр. K2Mg(CO3)2 4Н2О, из к-рых наиб. важен MgCa(CO3)2 (минерал доломит), бесцв. кристаллы с гексагoн. решеткой (а = 0,48079 нм, с = 1,16010 нм, z = 3, пространств. группа R3); плотн. 2,86 г/см3; твердость по Моосу 3,5-4.
Магнезит и доломит используют для получения разл. материалов с общим техн. назв. "магнезии" (см. Магния оксид), под к-рыми понимают не только MgO разл. плотности и дисперсности, но и основные М. к. Осн. потребители магнезита - пром-сть огнеупорных материалов (ок. 90% добываемого сырья) и цементная пром-сть. Кроме того, магнезит и доломит - исходное сырье для получения металлич. Mg и его соед., их используют также в качестве удобрений и для снижения кислотности почв. ); т. пл. 990 °С (с разл.); плотн. 3,0 г/см3; С0р 76,11 Дж/(моль.К); DH0пл 59 кДж/моль, DH0обр -1096 кДж/моль; S0298 65,09 Дж/(моль.К); твердость по Моосу 3,5-4,5. Начинает разлагаться до MgO при 350 °С, давление диссоциации 0,1 МПа достигается при ~650°С. Р-римость М.к. в воде в отсутствие СО2 ~ 0,5 мг/л, под давлением СО2 она сильно возрастает. В водном р-ре М.к. сильно гидролизуется, поэтому при действии р-ров карбонатов металлов на р-ры солей Mg в р-ре образуются основные карбонаты состава xMgCO3.yMg(OH)2.zH2O, a MgCO3 м. б. получен только при действии КНСО3 в присут. большого избытка СО2 в р-ре. Безводный М.к. встречается в природе в виде минерала магнезита.
В системе MgCO3-H2O кристаллизуются пента-, три- и моногидраты М.к. Пентагидрат MgCO3.5H2O (минерал ландсфордит) - бесцв. кристаллы с моноклинной решеткой (а = 1,2369 нм, b = 0,7520 нм, с = 0,7315 нм, b = 99,6°, z = 4, пространств. группа P21/m); плотн. 1,72 г/см3; DH0обр -2566,9 кДж/моль, DG0обр -2199,9 кДж/моль; р-римость 0,18 г в 100 г Н2О при 20°С. Тригидрат MgCO3.3H2O (минерал несквегонит) - бесцв. кристаллы с моноклинной решеткой (а = 1,2112 нм, b = 0,5365 нм, с = 0,7697 нм, b = 90,7°, z = 4, пространств. группа Р21/т); плотн. 1,84 г/см3; DH0обр -1977,0 кДж/моль; р-римость 0,11 г в 100 г Н2О при 20 °С. При нагр. пентагидрат переходит в тригидрат, а при 60-80°С образуется основной карбонат состава 4MgCO3.Mg(OH)2.5H2O, к-рый выше 200 °С начинает разлагаться до MgO.
При насыщении водной суспензии М.к. СО2 происходит растворение М.к. и образуется гидрокарбонат Mg(HCO3)2, существующий только в р-ре. При взаимод. MgCO3 с карбонатами щелочных и щел.-зем. металлов образуются плохо р-римые двойные карбонаты, напр. K2Mg(CO3)2 4Н2О, из к-рых наиб. важен MgCa(CO3)2 (минерал доломит), бесцв. кристаллы с гексагoн. решеткой (а = 0,48079 нм, с = 1,16010 нм, z = 3, пространств. группа R3); плотн. 2,86 г/см3; твердость по Моосу 3,5-4.
Магнезит и доломит используют для получения разл. материалов с общим техн. назв. "магнезии" (см. Магния оксид), под к-рыми понимают не только MgO разл. плотности и дисперсности, но и основные М. к. Осн. потребители магнезита - пром-сть огнеупорных материалов (ок. 90% добываемого сырья) и цементная пром-сть. Кроме того, магнезит и доломит - исходное сырье для получения металлич. Mg и его соед., их используют также в качестве удобрений и для снижения кислотности почв.
===
Исп. литература для статьи «МАГНИЯ КАРБОНАТ»: Позин М. Е., Технология минеральных солей, 4 изд., ч. 1, Л., 1974, с. 265; Карбонаты. Минералогия и химия, пер. с англ., М., 1987.
П. М. Чукуров.
Страница «МАГНИЯ КАРБОНАТ» подготовлена по материалам химической энциклопедии.
|
|
|
|

|
|
Куплю
19.04.2011 Белорусские рубли в Москве Москва 18.04.2011 Индустриальные масла: И-8А, ИГНЕ-68, ИГНЕ-32, ИС-20, ИГС-68,И-5А, И-40А, И-50А, ИЛС-5, ИЛС-10, ИЛС-220(Мо), ИГП, ИТД Москва 04.04.2011 Куплю Биг-Бэги, МКР на переработку. Москва |
Продам
19.04.2011 Продаем скипидар Нижний Новгород 19.04.2011 Продаем растворители Нижний Новгород 19.04.2011 Продаем бочки новые и б/у. Нижний Новгород |
|
|

