|
МEЙЕРА - ШУСТЕРА ПЕРЕГРУППИРОВКА,
изомеризация третичных и вторичных ацетиленовых спиртов в а, р-ненасыщенные
кетоны или альдегиды в присут. кислых катализаторов, напр.:
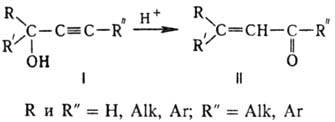
В М.-Ш.п. вступают спирты,
содержащие ОН-группу в a-положении к тройной связи (в т. ч. спирты с неск. кратными
связями) и ацетиленовые диолы. В качестве катализаторов обычно применяют неорг.
и орг. к-ты (напр., H2SO4, НСl, НСООН, ССl3СООН,
n-СН3С6Н4SО3Н), ацетилхло-рид,
ацетангидрид, тионилхлорид, фенол и др. Лучшие выходы получаются при использовании
в качестве р-рителей диоксана, ацетона, спиртов, сложных эфиров.
В случае первично-третичных
гликолей мигрирует гид-роксильная группа, связанная с третичным атомом С. У
гликолей с ароматич. и алифатич. заместителями происходит перемещение гидроксильной
группы, находящейся у атома С, несущего ароматич. заместитель.
Предполагаемый механизм
М.-Ш.п. включает 1-3-анио-нотропную миграцию в промежут. карбениевом ионе, напр.:
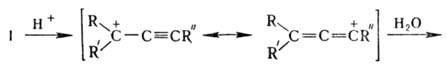
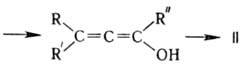
Побочные процессы - конденсация
исходных спиртов и их перегруппировки, автокон денсация продуктов р-ции (при
R: = Н). Последний процесс м. б. подавлен проведением р-ции в газовой фазе.
Перегруппировка открыта
К. Мейером и К. Шустером в 1922.
===
Исп. литература для статьи «МEЙЕРА - ШУСТЕРА ПЕРЕГРУППИРОВКА»: Вартанян С.
А., Баданян Ш. О., "Успехи химии", 1967, т. 36, в. 9, с. 1561-94;
Swaminathan S., Narayanan К. V., "Chem. Rev.", 1971, v. 71, № 5,
p. 429-38; Houben - Weyl, Methoden der organischen Chemie, 4 Aufl., Bd 7, Tl
2a, Stuttg., 1973, S. 907-26; Tapia O., Andres J., "Chem. Phys. Letters",
1984, v. 109, № 5, p. 471-77. К. В. Вацуро.
Страница «МEЙЕРА - ШУСТЕРА ПЕРЕГРУППИРОВКА» подготовлена по материалам химической энциклопедии.
|

