|
АРСЕНАТЫ (от лат. arsenicum - мышьяк), соли кислородсодержащих
к-т As. Различают A.(V) и А.(Ш) (устаревшее назв. - арсениты). Известны
А., в к-рых одновременно присутствуют As(III) и As(V), напр. Cr2As
As3O12.
A.(V) и А.(III)-производные соответствующих орто-мышъяковых (H3AsO4
и H3AsO3), метамышъяковых (HAsO3 и HAsO2)
и полимышьяковых (напр., H4As2O7 и H4As2O5,
H5As3O10, H2As4O7)
к-т; в своб. виде из указанных к-т получена только H3AsO4.
Наиб. распространены орто-арсенаты(V) и метаарсенаты(Ш), часто называемые
просто А. В основе структуры A.(V) лежат тетраэдры AsO4, причем
ортоарсенаты обычно построены из изолиров. тетраэдров, а метаарсенаты имеют
цепочечную или циклич. структуру (кольца из 3 или 4 тетраэдров, соединенных
вершинами). В основе структуры А.(Ш) лежат сплюснутые пирамиды AsO3,
к-рые могут соединяться в цепи через атомы О.
Гидро- и дигидроортоарсенаты(V) при нагр. отщепляют воду и превращ.
соотв. в пиро- и метаарсенаты(V). В кач-ве промежут. продуктов м. б. получены
и др. соединения, напр.: NaH2AsO4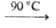 Na2H2As2O7
Na2H2As2O7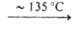
-> Na3H2As3O10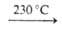 NaAsO3. При гидролизе мета- и пироарсенатов(V) образуются гидроарсенаты(V).
При высоких т-рах (около или выше т-ры плавления) метаарсенаты(V) разлагаются
до пироарсенатов(V), к-рые далее могут переходить в ортоарсенаты(V), обладающие
наиб. термич. устойчивостью. При термич. разложении последних могут образовываться
оксоарсенаты(V). Безводные А.(Ш) при 300-550°С диспропорционируют с образованием
A.(V) и As. Метаарсенаты(Ш) могут предварительно разлагаться до пиро- или
ортоарсенатов(Ш) с отщеплением As2O3.
NaAsO3. При гидролизе мета- и пироарсенатов(V) образуются гидроарсенаты(V).
При высоких т-рах (около или выше т-ры плавления) метаарсенаты(V) разлагаются
до пироарсенатов(V), к-рые далее могут переходить в ортоарсенаты(V), обладающие
наиб. термич. устойчивостью. При термич. разложении последних могут образовываться
оксоарсенаты(V). Безводные А.(Ш) при 300-550°С диспропорционируют с образованием
A.(V) и As. Метаарсенаты(Ш) могут предварительно разлагаться до пиро- или
ортоарсенатов(Ш) с отщеплением As2O3.
А. щелочных металлов, а также гидроарсенаты(V) щел.-зем. и нек-рых тяжелых
металлов раств. в воде, А.(Ш) щел.-зем. металлов малорастворимы, все остальные
А. практически не раств. в воде. А. разлагаются минер, к-тами и р-рами
щелочей. А.(Ш) в щелочных р-рах - сильные восстановители.
А. известны для всех металлов, кроме Аи и металлов платиновой группы.
Щелочные металлы образуют безводные мета-, пиро- и ортоарсенаты(V), плавящиеся
конгруэнтно, и триарсенаты, плавящиеся инконгруэнтно. Щел.-зем. и др. металлы
в степени окисления + 2 в отсутствие воды образуют мета-, пиро- и ортоарсенаты(V),
а также оксоарсенаты(V), напр. состава 6MO*As2O5.
Из А.(III) чаще других встречаются MII(AsO2)2
и MII3(AsO3)2.
Для элементов в степени окисления + 3 характерно образование
ортоарсенатов(V). А.(III), выделенные из водных р-ров, обычно имеют состав
M(AsO2)3*nН2О, полученные в отсутствие
воды - МАsО3. Для элементов в степени окисления + 4 характерны
гидроарсенаты(V) и пироарсенаты(V). Примеры A.(V) металлов в степени окисления
+ 5: NbOAsO4*4H2O и NbO(HAsO4)3
*5H2O.
Существуют двойные А., напр. М М AsO4, MIMIII
(AsO4)2. Из А., содержащих др. анионы, наиб. изучены
M5II(AsO4)3X, где Х-ОH-,
F-, Сl- и др. Известно ок. 85 прир. минералов, относящихся
к A.(V): скородит FeAsO4*2H2O, эритрин Co3(AsO4)2*8Н2О,
оли-венит Cu2AsO4(OH), миметизит Pbs(AsO4)3Cl
и др. Природные А.(III) - очень редкие минералы, напр. армангит Mn3(AsO3)2.
А. получают в осн. взаимод. оксидов As или р-ров мышьяковых к-т с оксидами,
гидроксидами или карбонатами металлов, А. тяжелых металлов - р-цией их
солей с Na3AsO4 или NaAsO2 (иногда с Li3AsO4
или LiAsO2) в р-ре. A.(V) синтезируют также окислением А.(III).
А.-диэлектрики или полупроводники с большой шириной запрещенной зоны.
Многие, напр. KH2AsO4 или арсенаты РЗЭ,-сегнето-
и пьезоэлектрики. Нек-рые А.-антиферромагнетики. Среди А. есть и твердые
электролиты, напр. Ag7I4AsO4, NaZr2(AsO4)3.
Гидроарсенат(V) натрия Na2HASO4*7Н2О-бесцв.
кристаллы; т. пл. 57°С (см также табл.); раств. в воде, спирте и глицерине,
не раств. в эфире. Получают нагреванием смеси As2O3
с NaNO3 с послед. гидролизом и перекристаллизацией из водного
р-ра или окислением р-ра NaAsO2 кислородом воздуха в присут.
CuSO4 либо анодным окислением. Инсектицид, антисептическое средство.
Дигидроарсенат(V) калия К.Н2АsО4 - бесцв. кристаллы,
решетка тетрагональная (а = 0,76290 нм, с = = 0,71612 нм, z = 4,
пространств, группы I42d); не раств. в спирте, раств. в воде и глицерине.
Это соединение, как и А. аммония, Rb, Cs, - материал нелинейной оптики.
СВОЙСТВА АРСЕНАТОВ
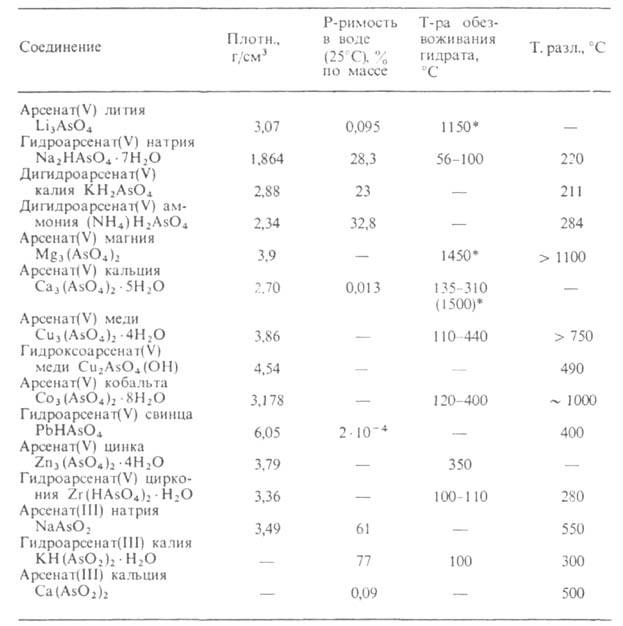
* Т-ра плавления безводной соли.
Гидроарсенат(V) свинца PbHAsO4 - белые кристаллы. Подобно
арсенатам Са, Zn, Cu, Mg- инсектицид и фунгицид, антисептич. ср-во для
пропитки древесины, компонент необрастающих красок для судов.
Арсенат(V) кобальта Co3(AsO4)2*8H2O
- розовые кристаллы. Пигмент для росписи на стекле и фарфоре, компонент
шихты в произ-ве цветного стекла.
Арсенат(Ш) кальция. Техн. продукт - смесь метаарсената(Ш) Ca(AsO2)2
с ортоарсенатом(Ш) Ca3(AsO3)2. Получают
взаимод. As2O3 с Са(ОН)2 при нагревании.
Инсектицид, бактерицидное ср-во, компонент смеси для протравливания семян,
необрастающих красок для судов.
Гидроксоарсенат(Ш) меди (зелень Шееле) Cu3(AsO3)2*nCu(OH)2*mН2О
(где и = 1 - 3) - желтовато-зеленое или темно-зеленое твердое в-во; не
раств. в воде и спирте. Получают взаимод. CuSO4, As2O3
и Na2CO3 в водном р-ре. Арсенат(Ш)-ацетат меди (парижская,
или швейнфуртская, зелень) Cu4(AsO2)6(CH3CO2)2
- изумрудно-зеленое твердое в-во; плотн. ~ 3,2 г/см3;
не раств. в воде и спирте, водой постепенно гидролизуется с отщеплением
As2O3. Получают взаимод. р-ров CuSO4,
CH3CO2Na и NaAsO2 или действием СН3СО2Н
и As2O3 на Сu2(ОН)2СО3
при нагревании. Оба соед. - инсектициды и фунгициды, компоненты необрастающих
красок для судов, пигменты для художеств. красок. А., в особенности водорастворимые,
- сильные яды.
===
Исп. литература для статьи «АРСЕНАТЫ»: Рцхиладзе В. Г., Мышьяк, М., 1969; Позин М. Е., Технология
минеральных солей ..., 4 изд., ч. 2, Л., 1974, с. 1396-1429; Keller P.,
"Neues Jahrbuch fur Mjneralogie Monatshefte", 1971, H. 11, S. 419-510.
П.И.Федоров.
Страница «АРСЕНАТЫ» подготовлена по материалам химической энциклопедии.
|

