|
ПРОПИЛЕНОКСИД (метилоксиран,
1,2-пропиленоксид), мол.м. 5,08; бесцв. прозрачная жидкость; т.пл. — 112°С,
т. tкриткип. 34,3°С, 0°С/210·мм рт. ст.; 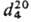 0,8311; 1,3660;
0,8311; 1,3660; 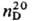 tкрит
209,15°С, ркрит 4,92 МПа; h 0,28 мПа·с (25 °С),
0,41 мПа·с (0°С); m 6,61·10-30 Кл·м: С_ 1,97 кДж/(кг·К);
tкрит
209,15°С, ркрит 4,92 МПа; h 0,28 мПа·с (25 °С),
0,41 мПа·с (0°С); m 6,61·10-30 Кл·м: С_ 1,97 кДж/(кг·К);
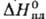 6,54 кДж/моль, 6,54 кДж/моль,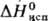 27,92 кДж/моль,
27,92 кДж/моль, 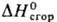 -191 кДж/моль,
-191 кДж/моль,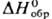 —92,82 кДж/моль (жидкость);
ур-ние температурной зависимости давления пара: lgp (мм. рт. ст.) = 1722,7/T+
+ 8,48 (243-306 К). Раств. в большинстве орг. р-рителей; в воде при 10 °С
раств. 40,8% по массе П., при 20 °С-40,1%. В П. при 10°С раств. 10,4%
Н2О, при 20°С-12,4%. При повыш. давлении П. с водой образует
азеогропы: т.кип. 69 °С (0,2 МПа, 0,1% по массе Н2О) и т.кип.
86,5 °С (0,4 МПа, 0,2% Н2О). При пониж. т-рах кристаллизуется
гидрат С3Н6О·16Н2О, т.пл. -3°С.
—92,82 кДж/моль (жидкость);
ур-ние температурной зависимости давления пара: lgp (мм. рт. ст.) = 1722,7/T+
+ 8,48 (243-306 К). Раств. в большинстве орг. р-рителей; в воде при 10 °С
раств. 40,8% по массе П., при 20 °С-40,1%. В П. при 10°С раств. 10,4%
Н2О, при 20°С-12,4%. При повыш. давлении П. с водой образует
азеогропы: т.кип. 69 °С (0,2 МПа, 0,1% по массе Н2О) и т.кип.
86,5 °С (0,4 МПа, 0,2% Н2О). При пониж. т-рах кристаллизуется
гидрат С3Н6О·16Н2О, т.пл. -3°С.
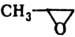
П.-один из наиб. распространенных
оксидов олефинов (см. Олефинов оксиды). Для него характерны р-ции присоединения,
обусловленные относит. легкостью размыкания цикла. Наиб. распространенная р-ция-гидратация
с образованием пропиленгликоля. Побочные продукты ди-, три-и полигликоли. Гидратация
П. с использованием СО2 (120-160 °С, 0,5-4 МПа) протекает селективно
с образованием монопропиленгликоля (кат.-четвертичные соли аммония и фосфония,
третичные амины, галогениды щелочных металлов); промежуточно образуется пропиленкарбонат
(I):
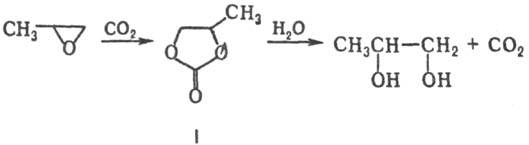
Со спиртами и фенолами
П. образует простые эфиры гликолей: в присут. щелочей-преим. первичный эфир,
в при-сут. к-т-смесь первичного и вторичного эфиров в равном отношении:
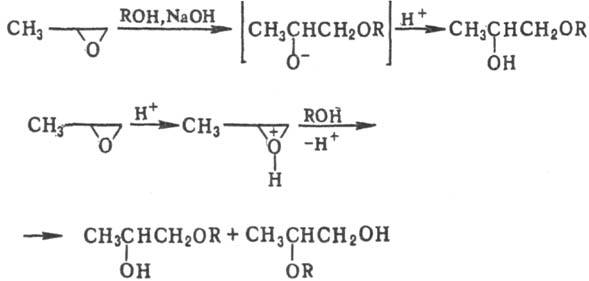
При взаимод. с карбоновыми
к-тами в присут. солей щелочных металлов П. превращ. в гидроксизамещенные сложные
эфиры; при взаимод. с галогеноводородами дает соответствующие галогенгидрины,
с NH3-моно-, ди- или триизопропаноламины. Гидрирование в присут.
N1 приводит к 1-пропанолу, восстановление амальгамой Na, Na в жидком NH3
или LiAlH4 - к изопропанолу. С альдегидами и кетонами П. образует
циклич. ацетали, с кетенами g-лактоны, напр.:
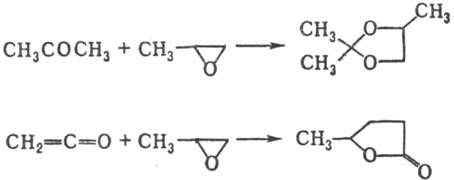
Изомеризация П. при 240-500
°С в присут. SiO2, A12O3, пемзы и др. катализаторов
идет с образованием смеси пропионового альдегида, ацетона и аллилового спирта.
В присут. разл. катализаторов
(щелочи, к-ты Льюиса, металлоорг. соед., амины, спирты, фенолы) П. легко поли-меризуется
в полипропиленоксид [—ОСН2СН(СН3)—]n
с мол. массой до неск. миллионов. Полимеризация П. в массе в присут. пропиленгликоля
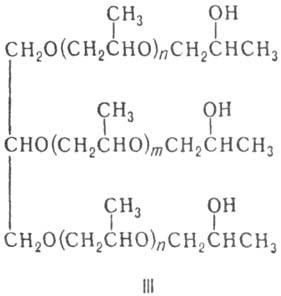
при 100-160°С приводит к поли-пропиленгликолю (ф-ла II); в присут. глицерина,
пента-эритрита или сорбита-к полиоксипропиленполиолам, напр. соед. III в случае
глицерина.
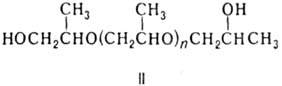
При сополимеризации с этиленоксидом
и пропиленгли-колем в присут. щелочных катализаторов или этилендиами-на П. образует
блоксополимеры - соотв. проксанолы или проксамины. В р-ре П. легко
сополимеризуется с аллилгли-цидовым эфиром с образованием пропиленоксидного
каучука.
Получают П. гл. обр. хлоргидринным
и пероксидным методами. Схема хлоргидринного метода:
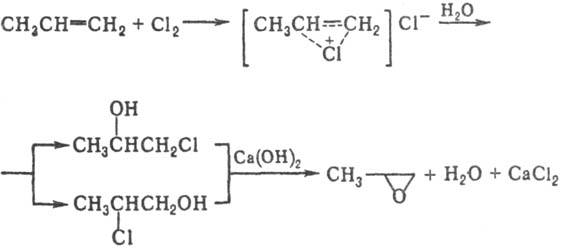
Пропилен и С12
смешивают в эквимолярных кол-вах с избытком Н2О (4-7-кратный); р-цию
проводят при 35-40 °С, поддерживая концентрацию пропиленхлоргидрина не более
4-6% по массе для уменьшения кол-ва побочных продуктов-дихлорпропана и дихлорпропилового
эфира. Избыток пропилена отделяют и возвращают в р-цию. На след. стадии при
комнатной т-ре водный р-р смеси пропи-ленхлоргидринов обрабатывают избытком
известкового молока-р-ра Са(ОН)2. Образующийся П. отгоняют для предотвращения
гидратации в гликоль. Недостаток процесса - использование С12 и образование
больших кол-в разб. (5-6%) р-ра СаС12. Наиб. экономичная разновидность
процесса - комбинирование с электролитич. произ-вом С12 и NaOH; при
этом гидролиз пропиленхлоргидрина осуществ-ляют при 80 °С р-ром
NaOH после электролиза, а образующийся р-р NaCl используют для растворения NaCl,
направляемого на электролиз.
Пероксидный способ синтеза
П. основан на окислении олефинов надкислотами (Прилежаева реакция)
и гидропероксидами
изобутана и этилбензола. В первом варианте синтеза П. образуется при взаимод.
пропилена с надуксус-ной или надпропионовой к-той, получаемыми окислением ацетальдегида
или пропионовой к-ты; соотв. этот вариант синтеза не находит широкого применения.
Второй вариант синтеза осуществляют по схемам 1 и 2:
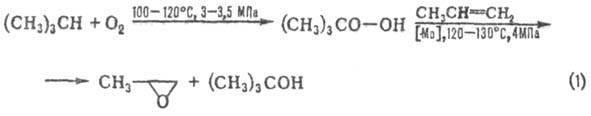
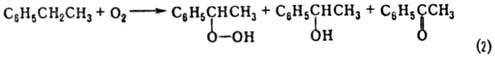
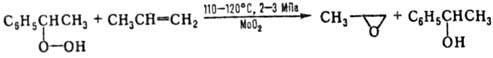
Селективность превращения
в П.-90-99%.
Иногда применяют также
эпоксидирование пропилена гидропероксидом пропилбензола (кумольный метод).
П.- исходное сырье для
получения пропиленгликоля, про-пиленкарбоната, изопропаноламинов, полиоксипропилен-полиолов,
полипропиленоксида, пропиленоксидных каучу-ков, пропиленсульфида, нек-рых ПАВ;
промежут. продукт в синтезе эфиров пропиленгликоля, эпихлоргидриновых кау-чуков,
полиуретанов и полиэфирных смол.
П.-горючая жидкость; КПВ
2,1-21,5% по объему. ПДК 1 мг/м3.
П. обладает цитотоксичным
и мутагенным действием, вызывает расстройства гемодинамики; ЛД50
580 мг/кг (мыши, внутрижелудочно).
Объем мирового произ-ва
ок. 3 млн.т/год (1987).
===
Исп. литература для статьи «ПРОПИЛЕНОКСИД»: Kirk - Othraer
encyclopedia, 3 ed., v. 19, N.Y., 1982, p. 246-74.
Б. Б. Чесноков.
Страница «ПРОПИЛЕНОКСИД» подготовлена по материалам химической энциклопедии.
|

