|
АТОМ (от греч. atomos - неделимый), наименьшая частица хим. элемента,
носитель его св-в. Каждому хим. элементу соответствует совокупность определенных
А. Связываясь друг с другом, А. одного или разных элементов образуют более
сложные частицы, напр. молекулы. Все многообразие хим. в-в (твердых, жидких
и газообразных) обусловлено разл. сочетаниями А. между собой. А. могут
существовать и в своб. состоянии (в газе, плазме). Св-ва А., в т. ч. важнейшая
для химии способность А. образовывать хим. соед., определяются особенностями
его строения.
Общая характеристика строения атома. А. состоит из положительно заряженного
ядра, окруженного облаком отрицательно заряженных электронов. Размеры А.
в целом определяются размерами его электронного облака и велики по сравнению
с размерами _ядра А^ (линейные размеры А. ~ 10~8см, его ядра
~ 10" -10" 13 см). Электронное облако А. не имеет строго определенных
границ, поэтому размеры А. в значит. степени условны и зависят от способов
их определения (см. Атомные радиусы). Ядро А. состоит из Z протонов
и N нейтронов, удерживаемых ядерными силами (см. Ядро атомное).
Положит. заряд протона и отрицат. заряд электрона одинаковы по абс.
величине и равны е= 1,60*10-19 Кл; нейтрон не обладает элек-трич.
зарядом. Заряд ядра +Ze - осн. характеристика А., обусловливающая его принадлежность
к определенному хим. элементу. Порядковый номер элемента в периодич. системе
Менделеева (атомный номер) равен числу протонов в ядре.
В электрически нейтральном А. число электронов в облаке равно числу
протонов в ядре. Однако при определенных условиях он может терять или присоединять
электроны, превращаясь соотв. в положит. или отрицат. ион, напр. Li+,
Li2+ или О-, О2-. Говоря об А. определенного
элемента, подразумевают как нейтральные А., так и ионы этого элемента.
Масса А. определяется массой его ядра; масса электрона (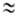 9,109*10-28
г) примерно в 1840 раз меньше массы протона или нейтрона ( 9,109*10-28
г) примерно в 1840 раз меньше массы протона или нейтрона (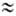 1,67*10-24 г), поэтому вклад электронов в массу А. незначителен.
Общее число протонов и нейтронов А = Z + N наз. массовым числом.
Массовое число и заряд ядра указываются соотв. верхним и нижним индексами
слева от символа элемента, напр. 2311Na. Вид атомов
одного элемента с определенным значением N наз. нуклидом. А. одного
и того же элемента с одинаковыми Z и разными N наз. изотопами этого
элемента. Различие масс изотопов мало сказывается на их хим. и физ. св-вах.
Наиболее значит, отличия (изотопные эффекты)наблюдаются у изотопов
водорода вследствие большой относит. разницы в массах обычного атома
1,67*10-24 г), поэтому вклад электронов в массу А. незначителен.
Общее число протонов и нейтронов А = Z + N наз. массовым числом.
Массовое число и заряд ядра указываются соотв. верхним и нижним индексами
слева от символа элемента, напр. 2311Na. Вид атомов
одного элемента с определенным значением N наз. нуклидом. А. одного
и того же элемента с одинаковыми Z и разными N наз. изотопами этого
элемента. Различие масс изотопов мало сказывается на их хим. и физ. св-вах.
Наиболее значит, отличия (изотопные эффекты)наблюдаются у изотопов
водорода вследствие большой относит. разницы в массах обычного атома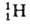 (протия), дейтерия D
(протия), дейтерия D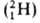 и трития Т
и трития Т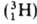 .
Точные значения масс А. определяют методами масс-спектрометрии. .
Точные значения масс А. определяют методами масс-спектрометрии.
Квантовые состояния атома. Благодаря малым размерам и большой массе
ядро А. можно приближенно считать точечным и покоящимся в центре масс А.
и рассматривать А. как систему электронов, движущихся вокруг неподвижного
центра - ядра. Полная энергия такой системы Е равна сумме кинетич.
энергий Т всех электронов и потенциальной энергии U, к-рая складывается
из энергии притяжения электронов ядром и энергии взаимного отталкивания
электронов друг от друга. А. подчиняется законам квантовой механики; его
осн. характеристика как квантовой системы - полная энергия Е - может
принимать лишь одно из значений дискретного ряда Е1 <
Е2 < Е3 < ...; промежут. значениями энергии
А. обладать не может. Каждому из "разрешенных" значений Е соответствует
одно или неск. стационарных (с не изменяющейся во времени энергией) состояний
А. Энергия Е может изменяться только скачкообразно - путем квантового
перехода А. из одного стационарного состояния в другое. Методами квантовой
механики можно точно рассчитать Е для одноэлектронных А. - водорода
и водородоподобных: Е= —hcRZ2/n2, где h
- постоянная Планка, с-скорость света, целое число п =
1, 2, 3, ... определяет дискретные значения энергии и наз. главным квантовым
числом; R-постоянная Ридберга (hcR = 13,6 эВ). При использовании
СИ ф-ла для выражения дискретных уровней энергии одноэлектронных А. записывается
в виде:
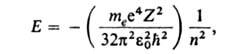
где те- масса электрона,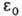 -электрич.
постоянная, -электрич.
постоянная,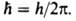 Возможные "разрешенные" значения энергии электронов в А. изображают в виде
схемы уровней энергии - горизонтальных прямых, расстояния между к-рыми
соответствуют разностям этих значений энергий (рис. 1). наиб. низкий уровень
E1, отвечающий минимально возможной энергии, наз. основным,
все остальные - возбужденными. Аналогично наз. состояния (основное и возбужденныеХ
к-рым соответствуют указанные уровни энергии. С ростом п уровни
сближаются и при
Возможные "разрешенные" значения энергии электронов в А. изображают в виде
схемы уровней энергии - горизонтальных прямых, расстояния между к-рыми
соответствуют разностям этих значений энергий (рис. 1). наиб. низкий уровень
E1, отвечающий минимально возможной энергии, наз. основным,
все остальные - возбужденными. Аналогично наз. состояния (основное и возбужденныеХ
к-рым соответствуют указанные уровни энергии. С ростом п уровни
сближаются и при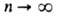 энергия электрона приближается к значению, отвечающему своб. (покоящемуся)
электрону, удаленному из А. Квантовое состояние А. с энергией Е полностью
описывается волновой ф-цией
энергия электрона приближается к значению, отвечающему своб. (покоящемуся)
электрону, удаленному из А. Квантовое состояние А. с энергией Е полностью
описывается волновой ф-цией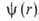 ,
где r-радиус-вектор электрона относительно ядра. Произведение ,
где r-радиус-вектор электрона относительно ядра. Произведение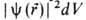 равно вероятности нахождения электрона в объеме dV, то есть
равно вероятности нахождения электрона в объеме dV, то есть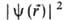 -плотность вероятности (электронная плотность). Волновая ф-ция
-плотность вероятности (электронная плотность). Волновая ф-ция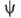 определяется уравнением Шрёдингера
определяется уравнением Шрёдингера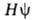 = =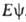 ,
где R-оператор полной энергии (гамильтониан). ,
где R-оператор полной энергии (гамильтониан).
Наряду с энергией движение электрона вокруг ядра (орбитальное движение)
характеризуется орбитальным моментом импульса (орбитальным мех. моментом)
М1; квадрат его величины может принимать значения, определяемые
орбитальным квантовым числом l = 0, 1, 2, ...;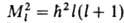 , где
, где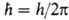 . При
заданном и квантовое число l может принимать значения от 0 до (и — 1).
Проекция орбитального момента на нек-рую ось z также принимает дискретный
ряд значений Мlz = . При
заданном и квантовое число l может принимать значения от 0 до (и — 1).
Проекция орбитального момента на нек-рую ось z также принимает дискретный
ряд значений Мlz =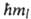 ,
где ml-магнитное квантовое число, имеющее дискретные значения
от — l до +l(-l,... - 1, О, 1, ... + l), всего 2l + 1 значений.
Ось z для А. в отсутствие внеш. сил выбирается произвольно, а в магн. поле
совпадает с направлением вектора напряженности поля. Электрон обладает
также собственным моментом импульса -спином и связанным с ним спиновым
магн. моментом. Квадрат спинового мех. момента МS2
= ,
где ml-магнитное квантовое число, имеющее дискретные значения
от — l до +l(-l,... - 1, О, 1, ... + l), всего 2l + 1 значений.
Ось z для А. в отсутствие внеш. сил выбирается произвольно, а в магн. поле
совпадает с направлением вектора напряженности поля. Электрон обладает
также собственным моментом импульса -спином и связанным с ним спиновым
магн. моментом. Квадрат спинового мех. момента МS2
=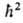 S(S +
+ 1) определяется спиновым квантовым числом S = 1/2, а проекция
этого момента на ось z Msz = = S(S +
+ 1) определяется спиновым квантовым числом S = 1/2, а проекция
этого момента на ось z Msz = =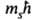 -квантовым
числом ms, принимающим полуцелые значения ms=1/2
и ms = -1/2. -квантовым
числом ms, принимающим полуцелые значения ms=1/2
и ms = -1/2.
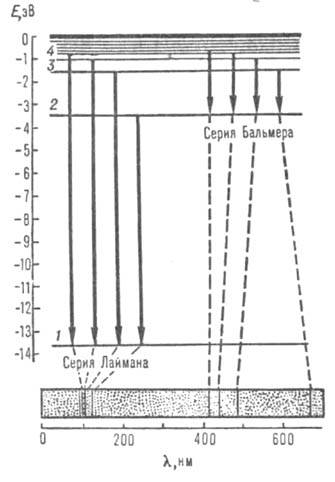
Рис. 1. Схема уровней энергии атома водорода (горизонтальные линии)
и оптич. переходов (вертикальные линии). Внизу изображена часть атомного
спектра испускания водорода - две серии спектральных линий; пунктиром показано
соответствие линий и переходов электрона.
Стационарное состояние одноэлектронного А. однозначно характеризуется
четырьмя квантовыми числами: п, l, ml и ms. Энергия
А. водорода зависит только от п, и уровню с заданным п соответствует
ряд состояний, отличающихся значениями l, ml, ms.
Состояния с заданными п и l принято обозначать как 1s, 2s, 2p,
3s и т.д., где цифры указывают значения л, а буквы s, p, d, f и
дальше по латинскому алфавиту соответствуют значениям д = 0, 1, 2,
3, ... Число разл. состояний с заданными п и д равно 2(2l+ 1) числу
комбинаций значений ml и ms. Общее число разл. состояний
с заданным п равно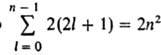 , т. е. уровням со значениями п = 1, 2, 3, ... соответствуют 2,
8, 18, ..., 2n2 разл. квантовых состояний. Уровень, к-рому соответствует
лишь одно квантовое состояние (одна волновая ф-ция), наз. невырожденным.
Если уровню соответствует два или более квантовых состояний, он наз. вырожденным
(см. Вырождение энергетических уровней). В А. водорода уровни энергии
вырождены по значениям l и ml; вырождение по ms имеет
место лишь приближенно, если не учитывать взаимод. спинового магн. момента
электрона с магн. полем, обусловленным орбитальным движением электрона
в электрич. поле ядра (см. Спин-орбитальное взаимодействие). Это
- релятивистский эффект, малый в сравнении с кулоновским взаимод., однако
он принципиально существен, т.к. приводит к дополнит. расщеплению уровней
энергии, что проявляется в атомных спектрах в виде т. наз. тонкой структуры.
, т. е. уровням со значениями п = 1, 2, 3, ... соответствуют 2,
8, 18, ..., 2n2 разл. квантовых состояний. Уровень, к-рому соответствует
лишь одно квантовое состояние (одна волновая ф-ция), наз. невырожденным.
Если уровню соответствует два или более квантовых состояний, он наз. вырожденным
(см. Вырождение энергетических уровней). В А. водорода уровни энергии
вырождены по значениям l и ml; вырождение по ms имеет
место лишь приближенно, если не учитывать взаимод. спинового магн. момента
электрона с магн. полем, обусловленным орбитальным движением электрона
в электрич. поле ядра (см. Спин-орбитальное взаимодействие). Это
- релятивистский эффект, малый в сравнении с кулоновским взаимод., однако
он принципиально существен, т.к. приводит к дополнит. расщеплению уровней
энергии, что проявляется в атомных спектрах в виде т. наз. тонкой структуры.
При заданных n, l и ml квадрат модуля волновой ф-ции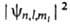 определяет для электронного облака в А. среднее распределение электронной
плотности. Разл. квантовые состояния А. водорода существенно отличаются
друг от друга распределением электронной плотности (рис. 2). Так, при l
= 0 (s-состояния) электронная плотность отлична от нуля в центре А. и не
зависит от направления (т.е. сферически симметрична), для остальных состояний
она равна нулю в центре А. и зависит от направления.
определяет для электронного облака в А. среднее распределение электронной
плотности. Разл. квантовые состояния А. водорода существенно отличаются
друг от друга распределением электронной плотности (рис. 2). Так, при l
= 0 (s-состояния) электронная плотность отлична от нуля в центре А. и не
зависит от направления (т.е. сферически симметрична), для остальных состояний
она равна нулю в центре А. и зависит от направления.

Рис. 2. Форма электронных облаков для различных состояний атома водорода.
В многоэлектронных А. вследствие взаимного электростатич. отталкивания
электронов существенно уменьшается прочность их связи с ядром. Напр., энергия
отрыва электрона от иона Не+ равна 54,4 эВ, в нейтральном атоме
Не она значительно меньше - 24,6 эВ. Для более тяжелых А. связь внеш. электронов
с ядром еще слабее. Важную роль в многоэлектронных А. играет специфич.
обменное взаимодействие, связанное с неразличимостью электронов,
и тот факт, что электроны подчиняются Паули принципу, согласно к-рому
в каждом квантовом состоянии, характеризуемом четырьмя квантовыми числами,
не может находиться более одного электрона. Для многоэлектронного А. имеет
смысл говорить только о квантовых состояниях всего А. в целом. Однако приближенно,
в т. наз. одноэлектронном приближении, можно рассматривать квантовые состояния
отдельных электронов и характеризовать каждое одноэлектронное состояние
(определенную орбиталъ, описываемую соответствующей ф-цией) совокупностью
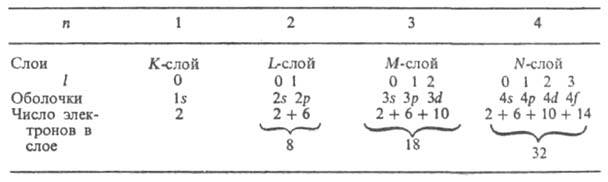
четырех квантовых чисел n, l, ml и ms. Совокупность
2(2l+ 1) электронов в состоянии с данными п и l образует электронную
оболочку (наз. также подуровнем, подоболочкой); если все эти состояния
заняты электронами, оболочка наз. заполненной (замкнутой). Совокупность
2п2 состояний с одним и тем же n, но разными l образует
электронный слой (наз. также уровнем, оболочкой). Для п= 1, 2, 3,
4, ... слои обозначают символами К, L, M, N, ... Число электронов
в оболочках и слоях при полном заполнении приведены в таблице:
Прочность связи электрона в А., т. е. энергия, к-рую необходимо сообщить
электрону, чтобы удалить его из А., уменьшается с увеличением п, а при
данном п - с увеличением l. Порядок заполнения электронами оболочек
и слоев в сложном А. определяет его электронную конфигурацию, т.е. распределение
электронов по оболочкам в основном (невозбужденном) состоянии этого А.
и его ионов. При таком заполнении последовательно связываются электроны
с возрастающими значениями и и /. Напр., для А. азота (Z = 7) и его ионов
N+, N2+, N3+, N4+, N5+
и N6+ электронные конфигурации имеют вид соотв.: Is22s22p3;
Is22s22p2; Is22s22p;
Is22s2; Is22s; Is2; Is (число
электронов в каждой оболочке указывается индексом справа сверху). Такие
же электронные конфигурации, как и у ионов азота, имеют нейтральные А.
элементов с тем же числом электронов: С, В, Be, Li, He, Н (Z = 6, 5, 4,
3, 2, 1). Начиная с n = 4 порядок заполнения оболочек изменяется: электроны
с большим п, но меньшим l оказываются связанными прочнее, чем электроны
с меньшим п и большим l (правило Клечковского), напр. 4s-электроны
связаны прочнее 3d-электронов, и сперва заполняется оболочка 4s, а затем
3d. При заполнении оболочек 3d, 4d, 5d получаются группы
соответствующих переходных элементов; при заполнении 4f- и 5f-оболочек
- соотв. лантаноиды и актиноиды. Порядок заполнения обычно соответствует
возрастанию суммы квантовых чисел (п + l); при равенстве
этих сумм для двух или более оболочек сначала заполняются оболочки с меньшим
и. Имеет место след. последовательность заполнения электронных оболочек:
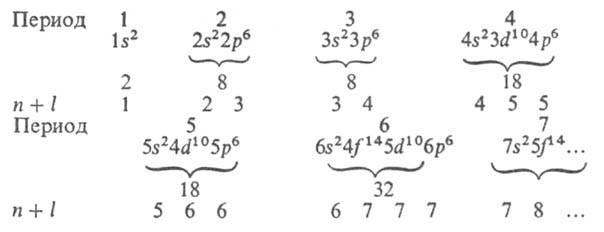
Для каждого периода указаны электронная конфигурация благородного газа,
макс. число электронов, а в последней строке приведены значения п +
l. Имеются, однако, отступления от этого порядка заполнения (подробнее
о заполнении оболочек см. Периодическая система химических элементов).
Между стационарными состояниями в А. возможны квантовые переходы.
При переходе с более высокого уровня энергии Еi на более
низкий Ek А. отдает энергию (Ei — Ek),
при обратном переходе получает ее. При излучательных переходах А. испускает
или поглощает квант электромагн. излучения (фотон). Возможны и безызлучательные
переходы, когда А. отдает или получает энергию при взаимод. с др. частицами,
с к-рыми он сталкивается (напр., в газах) или длительно связан (в молекулах,
жидкостях и твердых телах). В атомарных газах в результате столкновения
своб. А. с др. частицей он может перейти на др. уровень энергии - испытать
неупругое столкновение; при упругом столкновении изменяется лишь кинетич.
энергия постулат. движения А., а его полная внутр. энергия Е остается
неизменной. Неупругое столкновение своб. А. с быстро движущимся электроном,
отдающим этому А. свою кинетич. энергию, - возбуждение А. электронным ударом
- один из методов определения уровней энергии А.
Строение атома и свойства веществ. Хим. св-ва определяются строением
внеш. электронных оболочек А., в к-рых электроны связаны сравнительно слабо
(энергии связи от неск. эВ до неск. десятков эВ). Строение внеш. оболочек
А. хим. элементов одной группы (или подгруппы) периодич. системы аналогично,
что и обусловливает сходство хим. св-в этих элементов. При увеличении числа
электронов в заполняющейся оболочке их энергия связи, как правило, увеличивается;
наиб. энергией связи обладают электроны в замкнутой оболочке. Поэтому А.
с одним или неск. электронами в частично заполненной внеш. оболочке отдают
их в хим. р-циях. А., к-рым не хватает одного или неск. электронов для
образования замкнутой внеш. оболочки, обычно принимают их. А. благородных
газов, обладающие замкнутыми внеш. оболочками, при обычных условиях не
вступают в хим. р-ции.
Строение внутр. оболочек А., электроны к-рых связаны гораздо прочнее
(энергия связи 102-104 эВ), проявляется лишь при
взаимод. А. с быстрыми частицами и фотонами высоких энергий. Такие взаимод.
определяют характер рентгеновских спектров и рассеяние частиц (электронов,
нейтронов) на А. (см. Дифракционные методы). Масса А. определяет
такие его физ. св-ва, как импульс, кинетич. энергия. От механических и
связанных с ними магн. и электрич. моментов ядра А. зависят нек-рые тонкие
физ. эффекты (ЯМР, ЯКР, сверхтонкая структура спектральных линий, см Спектроскопия).
Более слабые по сравнению с хим. связью электростатич. взаимод. двух
А. проявляются в их взаимной поляризуемости - смещении электронов относительно
ядер и возникновении поляризац. сил притяжения между А. (см. Межмолекулярные
взаимодействия). А. поляризуется и во внеш. электрич. полях; в результате
уровни энергии смещаются и, что особенно важно, вырожденные уровни расщепляются
(см. Штарка эффект). А. может поляризоваться также под действием
электрич. поля волны электромагн. излучения; поляризация зависит от частоты
излучения, что обусловливает зависимость от нее показателя преломления
в-ва, связанного с поляризуемостью А. Тесная связь оптич. св-в А. с его
электрич. св-вами особенно ярко проявляется в оптич. спектрах.
Внеш. электроны А. определяют и магн. св-ва в-ва. В А. с заполненными
внеш. оболочками его магн. момент, как и полный момент импульса (мех. момент),
равен нулю. А. с частично заполненными внеш. оболочками обладают, как правило,
постоянными магн. моментами, отличными от нуля; такие в-ва парамагнитны
(см. Парамагнетики). Во внеш. магн. поле все уровни энергии А.,
для к-рых магн. момент не равен нулю, расщепляются (см. Зеемана эффект).
Все А. обладают диамагнетизмом, к-рый обусловлен возникновением у них
индуцированного магн. момента под действием внеш. магн. поля (см. Диэлектрики).
Св-ва А., находящегося в связанном состоянии (напр., входящего в состав
молекул), отличаются от св-в своб. А. наиб. изменения претерпевают св-ва,
определяемые внеш. электронами, принимающими участие в хим. связи; св-ва,
определяемые электронами внутр. оболочек, могут при этом практически не
изменяться. Нек-рые св-ва А. могут испытывать изменения, зависящие от симметрии
окружения данного атома. Примером может служить расщепление уровней энергии
А. в кристаллах и комплексных соед., к-рое происходит под действием электрич.
полей, создаваемых окружающими ионами или лигандами.
===
Исп. литература для статьи «АТОМ»: Карапетьянц М. X., Дракин С.И., Строение вещества, 3 изд.,
М., 1978; Шло лье кий Э. В., Атомная физика, 7 изд., т. 1-2, М., 1984.
М. А. Ельяшевич.
Страница «АТОМ» подготовлена по материалам химической энциклопедии.
|

