|
СИММОНСА-СМИТА РЕАКЦИЯ,
превращение алкенов в циклопропаны под действием метилиодида и пары Zn-Cu. Предполагают,
что активная частица в этой р-ции-иодид иодметилцинка (ф-ла I; реагент Симмон-са-Смита),
к-рый и переносит метиленовую группу на двойную связь, предположительно, путем
первоначального присоединения реагента и послед, отщепления ZnI2:
CH2I2 + Zn : ICH2ZnI
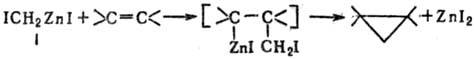
Пару Zn-Cu обычно получают
нагреванием Zn-пыли с CuCl в эфире в атмосфере N2. В эфире осуществляют
и основную р-цию.
Присоединение метилена
к двойной связи обычно происходит стереоспецифично; из транс-алкенов
образуются транс-циклопропаны, а из цис-алкенов - цис-циклопропаны.
В р-цию вступают алкены,
содержащие функц. группы,: причем выходы циклопропанов выше в случае алкенов
с электронодонорными группами. n-Метоксистирол дает соответствующий циклопропан
с выходом 70%, стирол -32%, винилацетат-31%, метиловый эфир кротоновой к-ты-9%.
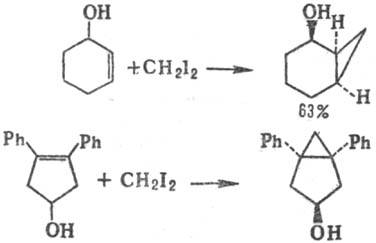
Присутствие в кольце ненасыщ.
алицикла гидроксигруппы оказывает ориентирующий эффект, а также приводит к существенному
ускорению р-ции и увеличению выходов, напр.:
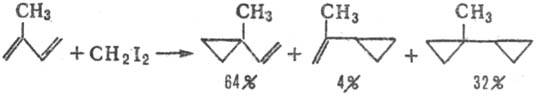
В случае диенов образуется
смесь продуктов, причем присоединение преим. идет по двойной связи, рядом с
к-рой имеется большее число алкильных групп:
Вместо меди м. б. использованы
галогениды меди (напр., CuCl) или серебро. Использование пары Zn-Ag обычно приводит
к более высоким выходам.
Р-ция открыта X. Симмонсом
и Р. Смитом в 1958.
===
Исп. литература для статьи «СИММОНСА-СМИТА РЕАКЦИЯ»: Физер Л.,
Физер М., Реагенты для органического синтеза, пер. с англ., т. 3, М., 1970,
с. 286-90; Марч Дж., Органическая химия, пер. с англ., т. 3, М., 1987, с. 269-70;
Simmons H. E. [а. о.], в кн.: Organic reactions, v. 20, N.Y.-L., 1973.
В. В. Жданкин.
Страница «СИММОНСА-СМИТА РЕАКЦИЯ» подготовлена по материалам химической энциклопедии.
|

