|
АЦЕТОН (от лат. acetum - уксус) (2-пропанон, диметилкетон) СН3СОСН3,
мол. м. 58,079; летучая бесцв. жидкость с характерным запахом; т. пл. —
94,6°С, т. кип. 56,1 °С; d420 0,7920, nD20
1,3588;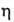 0,36 мПа*с (10°С), 0,30 мПа*с (30 С);
0,36 мПа*с (10°С), 0,30 мПа*с (30 С);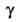 0,0237 Н/м (20°С); tкрит 235,5°С, pкрит 4,75
МПа; С°р 749,3 Дж/(кмоль*К);
0,0237 Н/м (20°С); tкрит 235,5°С, pкрит 4,75
МПа; С°р 749,3 Дж/(кмоль*К);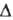 H°исп
29,1 кДж/моль (56,1 °С), H°исп
29,1 кДж/моль (56,1 °С), Н°сгор
-1787кДж/моль, Н°сгор
-1787кДж/моль,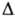 Н°обр
- 216,5 кДж/моль (газ; 25°С) и — 248 кДж/моль (жидкость). Смешивается с
водой и орг. р-рителями, напр. эфиром, метанолом, этанолом, сложными эфирами. Н°обр
- 216,5 кДж/моль (газ; 25°С) и — 248 кДж/моль (жидкость). Смешивается с
водой и орг. р-рителями, напр. эфиром, метанолом, этанолом, сложными эфирами.
А. обладает всеми хим. св-вами, характерными для алифатич. кетонов.
Образует кристаллич. соед. с гидросульфитами щелочных металлов, напр.
с NaHSO3 - (CH3)2C(OH)SO3Na.
Только сильные окислители, напр. щелочной р-р КМnО4 и хромовая
к-та, окисляют А. до уксусной и муравьиной к-т и далее - до СО2
и воды. Каталитически восстанавливается до изопропанола, амальгамами Mg
или Zn, а также Zn с СН3СООН - до пинакона (СН3)2С(ОН)С(ОН)(СН3)2.
Атомы водорода легко замещаются при галогенировании, нитрозировании и т.п.
Действием хлора и щелочи А. превращ. в хлороформ, к-рый взаимод. с А. с
образованием хлорэтона (СН3)2С(ОН)СС13,
применяемого как антисептик. А. окисляет вторичные спирты в присут. алкоголятов
А1 до кетонов (р-ция Оппенауэра):
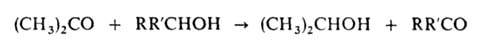
Вступает в альдольную конденсацию с образованием диацетонового спирта
(СН3)2С(ОН)СН2СОСН3, а также
в кротоновую конденсацию с образованием окиси мезитила (СН3)2С=СНСОСН3,форона(СН3)2С=-СНСОСН=С(СН3)2
и мезитилена. В присут. сильной минер. к-ты А. алкилирует фенол с
образованием дифенилолпропана (бисфенола А.) (НОС6Н4)2С(СН3)2,
присоединяет цианид-ион с образованием ацетонциангидрина (CH3)2C(OH)CN.
При пиролизе (700°С) А. образуются кетен СН2—С—О и метан.
В пром-сти А. получают преим. т. наз. кумольным способом одновременно
с фенолом из бензола и пропилена через изопропилбензол (кумол) по схеме:
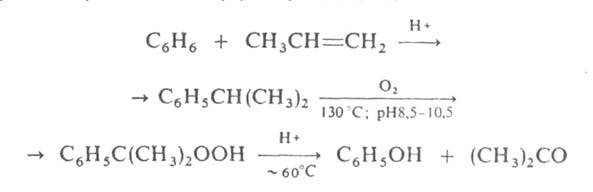
В ряде других пром. способов синтеза А. исходят из изопропанола:
1. Окисление в паровой фазе (кат. - металлич. Си, Ag, Ni или Pt):
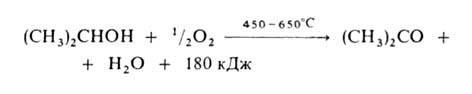
Высокий выход А. (ок. 90%) достигается при использовании Ag, осажденного
на пемзе, или серебряной сетки.
2. Автокаталитич. окисление в жидкой фазе при 90-140°С и 0,2-0,3 МПа:

Выход А. 95% от теоретического, Н2О2 87%.
3. Дегидрирование в паровой фазе в присут. ZnO, осажденной на пемзе:
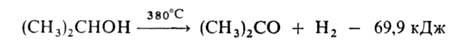
Степень превращ. изопропанола в А. при 225 °С составляет 84% при 380°С
- 98%, при 525°С - 100%. Выход А. около 90%.
Новый пром. способ получения А. - прямое окисление пропилена в жидкой
фазе в присут. PdCl2 в среде водного р-ра солей Pd, Fe или Си
при 50-120 °С и 5-10 МПа:
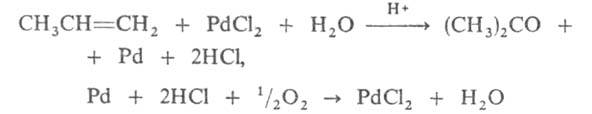
Выход А. 90%. Нек-рое значение сохранил способ получения А. брожением
крахмала под влиянием бактерий Bacyllus acetobutylicus, превращающих крахмал
в А. и бутанол (т. наз. ацетоновое брожение). Известны и др. способы получения:
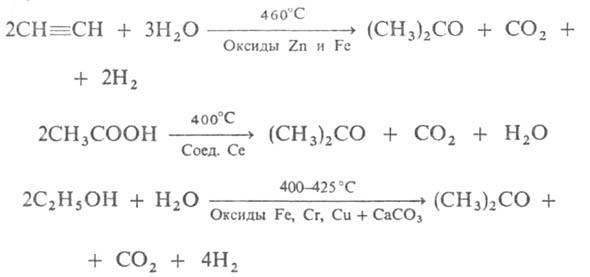
Старый пром. метод получения А.-сухая перегонка (СН3СОО)2Са
- потерял значение.
Для качеств. определения А. используют цветные р-ции, напр. с динитробензолом,
нитропруссидом Na (реактив Легаля); для идентификации - кристаллич. производные
А., напр. семикарбазон (т. пл. 187°С). Количественно А. определяют: 1)
оксимированием:
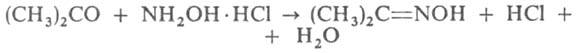
образующийся НCl титруют щелочью; 2) титрованием р-ром КМnО4
в щелочной среде (при этом А. окисляется до СО2 и Н2О).
А. - широко применяемый р-ритель орг. в-в, в первую очередь нитратов
и ацетатов целлюлозы; благодаря сравнительно малой токсичности он используется
также в пищ. и фармацевтич. пром-сти; А. служит также сырьем для синтеза
уксусного ангидрида, кетена, диацетонового спирта, окиси, мезитила, метилизобутилкетона,
метилметакрилата, дифенилолпропана, изофорона и многих др. соединений.
Мировое произ-во А. ок. 3 млн. т/год (1980).
Для А. т. всп. -20°С, т. самовоспл. 500°С; КПВ 2,15-13,00%. А. при вдыхании
накапливается в организме. Т.к. выводится из организма медленно, возможны
хронич. отравления. ПДК 200 мг/м3.
===
Исп. литература для статьи «АЦЕТОН»: Кружалов Б. Д., Голованенко Б. И., Совместное получение
фенола и ацетона, М, 1963; Теддер Дж., Нехватал А., Джубб А., Промышленная
органическая химия, пер. с англ., М., 1977; Kirk-Othmer encyclopedia, 3
ed., v. 1. N.Y.. 1978, p. 179-91. Ю.Н.Юрьев.
Страница «АЦЕТОН» подготовлена по материалам химической энциклопедии.
|

