|
СТРОНЦИЯ НИТРАТ Sr(NO3)2,
бесцв. кристаллы кубич. сингонии (а = 0,781 нм, z = 4, пространств.
группа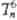 ); т.
пл. 645 °С (с разл.); плотн. 3,0 г/см3; ); т.
пл. 645 °С (с разл.); плотн. 3,0 г/см3; 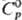 149,91 Дж/(моль·К);
149,91 Дж/(моль·К); 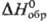 — 984,08 кДж/моль;
— 984,08 кДж/моль; 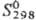 194,6 Дж/(моль·К); р-римость
в воде (г в 100 г): 70,5 (20 °С), 90,0 (40 °С) и 98,0 (80 °С). Из
водных р-ров до 29 °С при концентрации 47,0% по массе кристаллизуется тетрагидрат
Sr(NO3)2·4Н2О, а вышебезводный С.н.; т.пл.
криогидрата — 5,4 °С (24,7% по массе С.н.). Тетрагидрат-бесцв. кристаллы
моноклинной сингонии; плотн. 2,2 г/см3;
194,6 Дж/(моль·К); р-римость
в воде (г в 100 г): 70,5 (20 °С), 90,0 (40 °С) и 98,0 (80 °С). Из
водных р-ров до 29 °С при концентрации 47,0% по массе кристаллизуется тетрагидрат
Sr(NO3)2·4Н2О, а вышебезводный С.н.; т.пл.
криогидрата — 5,4 °С (24,7% по массе С.н.). Тетрагидрат-бесцв. кристаллы
моноклинной сингонии; плотн. 2,2 г/см3; 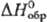 -2161,0 кДж/моль;
-2161,0 кДж/моль;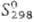 364 Дж/(моль · К); выше 100°С отщепляет воду с образованием безводного С.
н. В водных р-рах С. н. диссоциирует и слабо гидролизуется и образует нитратные
комплексы [Sr(H2O)3(NO3)3]-.
Получают С.н. растворением Sr, SrО, Sr(ОН)2 или SrCO3
в р-рах HNO3. С.н.-компонент пиротехн. составов для сигнальных, осветит.
и зажигат. ракет, окрашивающий пламя в карминово-красный цвет, компонент составов
для обезвреживания выхлопных газов автомобилей. П.М. Чукуров.
364 Дж/(моль · К); выше 100°С отщепляет воду с образованием безводного С.
н. В водных р-рах С. н. диссоциирует и слабо гидролизуется и образует нитратные
комплексы [Sr(H2O)3(NO3)3]-.
Получают С.н. растворением Sr, SrО, Sr(ОН)2 или SrCO3
в р-рах HNO3. С.н.-компонент пиротехн. составов для сигнальных, осветит.
и зажигат. ракет, окрашивающий пламя в карминово-красный цвет, компонент составов
для обезвреживания выхлопных газов автомобилей. П.М. Чукуров.
===
Исп. литература для статьи «СТРОНЦИЯ НИТРАТ»: нет данных
Страница «СТРОНЦИЯ НИТРАТ» подготовлена по материалам химической энциклопедии.
|

