|
СУЛЬФИТЫ
ОРГАНИЧЕСКИЕ, эфиры сернистой к-ты общей ф-лы ROS(O)OR', где R
= Н, Alk, Аг, R' = Alk, Аг. Различают симметричные (R и R' одинаковые), несимметричные,
или смешанные (R и R'paзличныe), и циклические С. о. Известны также производные
С. о.: хлорсульфиты ROS(O)C1, аминосульфиты RR'NS(O)OR:,
тиолсульфиты RSS(O)OR', дитиолсульфиты RSS(O)SR'.
Как правило, С. о. с открытой
цепью-бесцв. жидкости с резким запахом и лакриматорным действием; высшие С.
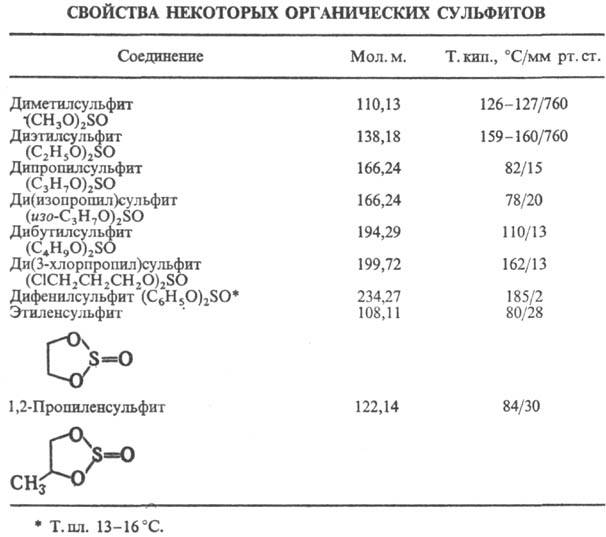
о.-вязкие масла, циклические-твердые легкоплавкие в-ва (см. табл.). Монозамещенные
сульфиты ROS(O)OH неустойчивы, стабильны их соли.
Конфигурация сульфитной
группы близка к тетраэдру с атомом S в одной из вершин. И К спектры С. о. имеют
характеристич. полосы в области 1200 см-1 (R и R' = алкил) и 1245
см-1 (R и R' = арил), соответствующие валентным колебаниям группы
S=O.
Основной и кислотный гидролиз
С. о. протекает с расщеплением связи S—О; скорость гидролиза циклических и арилсульфитов
выше, чем алкилсульфитов; повыш. чувствительностью к гидролизу обладает этиленсульфит.
Окисление С. о. КМnО4
приводит к сульфатам; при действии хлора на С. о. разрывается связь S—О и образуется
алкилхлорсульфонат и алкилхлорид:
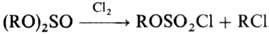
Подобно орг. сульфатам,
С. о. - алкилирующие агенты. Этиленсульфит используют вместо этиленоксида в
р-циях гидроксиэтилирования, напр.:
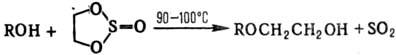
Со спиртами в присут. к-т
или оснований происходит переэтерификация С. о.; третичные спирты в р-цию не
вступают..
При взаимодействии С. о.
с аминокислотами образуются эфиры аминокислот: PhCH2CH(NH2)COOH
+ (CH3O)2SO :
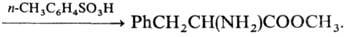
Р-ция n-нитрофенилсульфитов
с карбоксилат-ионом приводит к сложным эфирам (n-O2NC6H4O)2SO
+ RCOO : : n-O2NC6H4OC(O)R;
в случае несимметричных соед. [O2NC6H4OS(O)OR,
где R = О2Н5, Ph] карбоксилат-ион атакует нитрофенильную
группу.
При действии на диалкилсульфиты
SeO2 образуются диалкилселениты (RO)2SeO; при действии
SF4 одна из алкоксигрупп замещается на атом F.
При нагревании С. о. подвергаются
десульфированию с образованием простых эфиров или олефинов в зависимости от
наличия в молекуле С. о. bvH-атома, напр.:
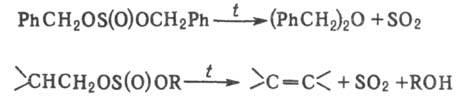
Диметилсульфит в присут.
катализаторов (напр., третичных аминов) изомеризуется в метилметансульфонат
CH3SO2OCH3.
Получают С. о. р-цией тионилхлорида
со спиртами в пиридине, напр.:
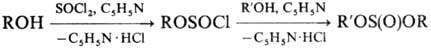
Иногда используют SO2
в пиридине в присут. I2 или Вг2.
Диалкилсульфиты образуются
при нагр. аддукта этилен-оксида и SO2 с первичными спиртами в присут.
гидридов щелочных металлов. Метилалкилсульфиты м.б. получены действием диазометана
на р-р SO2 в соответствующем спирте. Для синтеза нек-рых С. о. используют
р-цию пе-реэтерификации.
Смешанные алкил- и арилсульфиты
применяют в качестве инсектицидов и биоцидов; диэтилсульфит-для удаления остатков
катализатора при произ-ве полипропилена. Эти-ленсульфит-ускоритель в произ-ве
аминопластов; полисульфит структуры [ —OS(O)OCH2—]n-
компонент фотоэмульсий.
===
Исп. литература для статьи «СУЛЬФИТЫ ОРГАНИЧЕСКИЕ»: Woerden H.F.
van, "Chem. Rev.", 1963, v. 63, №6, p. 557-71; Kirk-Othmer
encyclopedia, 3 ed., v. 22, 1983. N. Y., p. 233. H.A. Тилькунова.
Страница «СУЛЬФИТЫ ОРГАНИЧЕСКИЕ» подготовлена по материалам химической энциклопедии.
|

