|
ТЕТРАНИТРОМЕТАН
C(NO2)4, мол.м. 196,04; бесцв. жидкость с резким запахом;
т.пл. 14,2 °С, т. кип. 125,7°С (со слабым разл.); 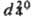 1,63944;
1,63944; 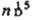 1,44066;
h 1,77мПа·с; 1,44066;
h 1,77мПа·с; 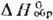 - 37,29 кДж/моль,
- 37,29 кДж/моль,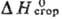 — 438,27 кДж/моль. Раств. в большинстве орг. р-рителей и конц. HNО3,
не раств. в воде, H2SO4 и многоатомных спиртах; перегоняется
с водяным паром.
— 438,27 кДж/моль. Раств. в большинстве орг. р-рителей и конц. HNО3,
не раств. в воде, H2SO4 и многоатомных спиртах; перегоняется
с водяным паром.
Т.-сильный окислитель.
С горючими (гл: обр. орг.) в-вами образует взрывчатые смеси, по мощности и чувствительности
превосходящие нитроглицерин. Чистый Т.-слабое ВВ; чувствительность к мех. воздействиям
незначительна, но резко возрастает при попадании малейших примесей орг. в-в;
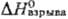 — 1915 кДж/моль;
объем газообразных
продуктов взрыва 670 л/кг; скорость детонации 6400 м/с в стальной трубе диаметром
21 мм. — 1915 кДж/моль;
объем газообразных
продуктов взрыва 670 л/кг; скорость детонации 6400 м/с в стальной трубе диаметром
21 мм.
Т. легко гидролизуется
водой или спиртовыми р-рами щелочей с образованием соотв. тринитрометана или
его солей, действие водных щелочных р-ров приводит к разложению Т.:
C(NO2)4
+ Н2О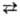 СH(NO2)3
+ HNО3, СH(NO2)3
+ HNО3,
C(NO2)4
+ КОН + C2H5OH : : C(NO2)3
К + C2H5ONO2 + Н2O,
C(NO2)4
+ 6КОН : К2СО3 + 4KNO2 + 3H2O.
В присут. щелочи и пиридина
Т. нитрует ароматич. соединения. Т. корродирует Си и его сплавы, Fe, не корродирует
Аl, нержавеющие стали, не взаимод. со стеклом. При добавлении к Т. ~ 0,2% по
массе H2SO4 его можно длительно хранить и транспортировать
в стальной таре.
Получают Т. деструктивным
нитрованием ацетилена [кат.-Hg(NO3)2], кетена или уксусного
ангидрида конц. HNO3.
Т.-сырье для получения
тринитрометана, нитрующий агент в лаб. практике.
===
Исп. литература для статьи «ТЕТРАНИТРОМЕТАН»: Орлова Е.
Ю., Химия и технология бризантных взрывчатых веществ, Л., 1981, с. 195-97.
А.Е. Фогельзанг.
Страница «ТЕТРАНИТРОМЕТАН» подготовлена по материалам химической энциклопедии.
|

