|
ФЕНИЛЕНДИАМИНЫ (диаминобензолы),
мол.м. 108,14; бесцв. кристаллы (табл.), темнеющие на свету и на воздухе. Существуют
в виде трех изомеров: 1,2-, 1,3- и 1,4-Ф. (соотв. о-, м- и n-F.).
Раств. в этаноле, диэтиловом эфире, CHCl3, горячей воде.
СВОЙСТВА ФЕНИЛЕНДИАМИНОВ
*d8020
1,1421, n57,7D 1,6339.
По хим. св-вам Ф.- типичные
представители ароматич. аминов. Сильные орг. основания; м-и n-F.
с минер, к-тами образуют водораство римые соли (за исключением сульфата
n-Ф.), с карбоновыми к-тами, их ангидридами и хлорангидридами -замещенные
амиды соответствующих к-т, с дикарбоновыми к-тами, диангидридами и дихлорангидридами
- полиамиды и полиимиды. При взаимод. с бензальдегидом Ф. дают
моно- и дибензилиденпроизводные.
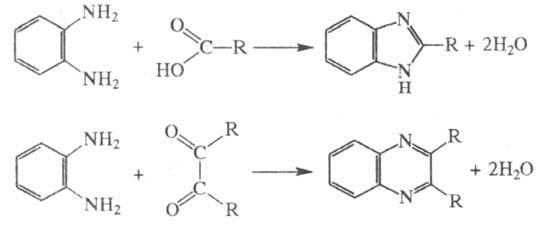
о-Ф. легко образует гетероцик-лич. соед.: взаимод. с к-тами, ангидридами,
амидами и эфи-рами приводит к бензимидазолам, с 1,2-дикарбонильными соед.- к
хиноксалинам:
м- и n-Ф.
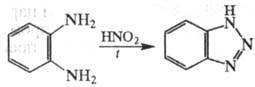
легко диазотируются HNO2 по одной или двум аминогруппам, образуя
диазо- и тетраазопроизводные - про-межут. продукты в произ-ве азокрасителей;
о-Ф. в аналогичных условиях дает бензотриазол:
При окислении действием
Ag2O в эфирном р-ре о- и м-Ф. превращается в соответствующие
бензохинондиимины; MnO2 или K2Cr2O7
в H2SO4 окисляют п-Ф. в n-бензохинон; при
окислении о-Ф. FeCl3 в CH3COOH образуется 2,3-диамино-феназин.
Окисление n-F. окислителями в присут. соед. с активной метиленовой
группой приводит к азометиновым красителям. В цветной фотографии используют
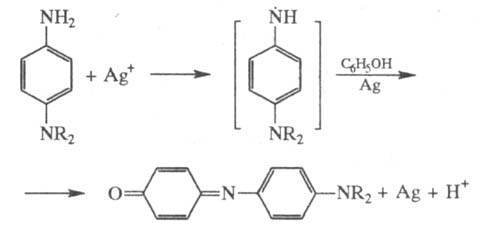
одноэлект-ронное окисление N,N-диалкилпроизводных n-F.
светочувст-вит. солями AgHaI; образующиеся радикалы с разл. агентами, напр,
фенолами, дают индоанилиновые красители:
В присут. своб. радикалов
или соед., являющихся источниками своб. радикалов (Br2, Cl2,
H2O2, O3), n-F. и его производные
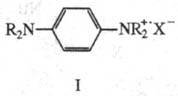
способны превращаться в окрашенные катион-радикалы (соли Вюрстера, ф-ла I),
применяемые в качестве антиоксидантов, ингибиторов полимеризации, красителей
в цветной фотографии.
При действии Cl2
в CH3COOH или KClO4 в HCl n-F. превращается
в тетрахлор-n-бензохинон (хлоранил); м-Ф. при нагр. с 10%-ным
р-ром HCl образует резорцин, м- и n-F. легко сополимеризуются
с разл. орг. соед.; напр., с диизоцианатами образуют полиуретаны, с диальдегидами
- полишиффовы основания, с эпоксидами - сетчатые полимеры.
В пром-сти о-Ф. получают
восстановлением о-нитроанили-на NaHS (реже - Zn-пылью в водно-спиртовом
р-ре NaOH) или его каталитич. гидрированием в присут. Pd/C (70-90 0C,
3 МПа, выход 85-90%) или Ni/Cr2O3; м-Ф.- восстановлением
м-динитробензола порошком Fe в HCl (выход 74%) или его каталитич. гидрированием
в присут. Ni; n-F.- восстановлением n-нитроанилина Na2S,
порошком Fe в HCl или Zn в KOH. Другие способы получения: взаимод. соответствующих
дибромбензолов с водным NH3 в присут. CuSO4 при 175-180
0C (о-Ф.)и 180-190 0C (n-F.); восстановление
n-нит-роанилина на Cu-Mo-катализаторе в присут. небольших кол-в NH4Cl
или CH3COOH.
Ф.- реагенты в произ-ве
кубовых красителей (о-Ф.), азокрасителей (м-Ф.), сернистых, прямых
и дисперсных красителей (n-F.); соли Ф.- проявляющие в-ва в черно-белой
и цветной фотографии, м- и n-F. используют в произ-ве полиамидов,
полиуретанов, в качестве антиоксидантов и антиозо-нантов пластмасс и эластомеров,
отвердителей эпоксидных смол (м-Ф.), для окрашивания волос и меха (n-F.),
как реагенты для обнаружения моносахаридов (n-F.), хлора, брома,
озона (n-Ф.).
Ф.- токсичны; неблагоприятно
действуют на почки, печень, изменяют состав крови, вызывают респираторные заболевания
и дерматиты. ПДК в воздухе рабочей зоны для о-, м- и n-F.
соотв. 0,5, 0,1 и 0,05 мг/м3; для n-F. ЛД50
133,4 мг/кг (крысы, перорально). Ниж. КПВ для о-Ф. 10,4 г/м3.
T. всп. для n-Ф. 155,5 0C.
===
Исп. литература для статьи «ФЕНИЛЕНДИАМИНЫ»: Общая органическая
Страница «ФЕНИЛЕНДИАМИНЫ» подготовлена по материалам химической энциклопедии.
|

