|
ФЛУОРЕН
(о,о'-дифениленметан), ф-ла I, мол.м. 166,2; бесцв. кристаллы, флуоресцирующие
в УФ свете; т. пл. 116-117 оC, т.кип. 293-295 оC; 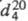 1,181;
1,181; 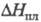 121 кДж/кг; 121 кДж/кг;
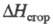 -39940 кДж/кг; m
1,9347 · 10-30 Кл · м; рКа 22,9. Хорошо раств.
в диэтиловом эфире, плохо - в этаноле, не раств. в воде. Ф. окисляется кислородом
воздуха до 9-гидропероксифлуо-рена, K2Cr2O7
в CH3COOH - до флуоренона (II, т. пл. 84 оC, т. кип. 342
0C), HI и красным P восстанавливается до пергид-рофлуорена. Легко
образует карбанион по атому С-9: при конденсации с ароматич. альдегидами дает
9-арилиденфлуо-рены, при нагр. с Na или NaNH2 - 9-натрийпроизводное,
с акрилонитрилом и бензилхлоридом в присут. катализатора -соответствующие 9,9-дизамещенные.
Электроф. замещение происходит предпочтительно по положению 2: галогенирова-ние
SO2Cl2 или Cl2 в CH3Cl на холоде
приводит к 2-хлор-флуорену, дальнейшее хлорирование - к 2,7-дихлор- и 2,4,7-трихлорфлуоренам,
нитрование - к 2-нитропроизвод-ному, сульфирование - к 2-сульфо- и 2,7-дисульфопроизвод-ным.
С динитробензолом, тринитротолуолом, пикриновой к-той Ф. образует мол. соед.
(т. пл. пикрата 80-82 0C). -39940 кДж/кг; m
1,9347 · 10-30 Кл · м; рКа 22,9. Хорошо раств.
в диэтиловом эфире, плохо - в этаноле, не раств. в воде. Ф. окисляется кислородом
воздуха до 9-гидропероксифлуо-рена, K2Cr2O7
в CH3COOH - до флуоренона (II, т. пл. 84 оC, т. кип. 342
0C), HI и красным P восстанавливается до пергид-рофлуорена. Легко
образует карбанион по атому С-9: при конденсации с ароматич. альдегидами дает
9-арилиденфлуо-рены, при нагр. с Na или NaNH2 - 9-натрийпроизводное,
с акрилонитрилом и бензилхлоридом в присут. катализатора -соответствующие 9,9-дизамещенные.
Электроф. замещение происходит предпочтительно по положению 2: галогенирова-ние
SO2Cl2 или Cl2 в CH3Cl на холоде
приводит к 2-хлор-флуорену, дальнейшее хлорирование - к 2,7-дихлор- и 2,4,7-трихлорфлуоренам,
нитрование - к 2-нитропроизвод-ному, сульфирование - к 2-сульфо- и 2,7-дисульфопроизвод-ным.
С динитробензолом, тринитротолуолом, пикриновой к-той Ф. образует мол. соед.
(т. пл. пикрата 80-82 0C).
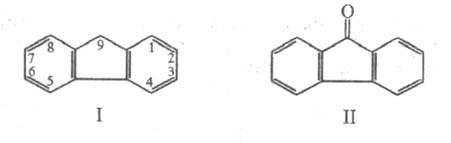
Ф. содержится в кам.-уг.
смоле (1,3-2%); выделяется из ее антраценовой фракции (210-308 0C)
кристаллизацией с послед. перекристаллизацией из бензина. Препаративные способы
получения - пиролиз ацетилена, пропускание паров дифенилметана через раскаленную
трубку.
Ф.- исходный продукт для
получения красителей, стабилизатор полимеров. Монокристаллы Ф. применяют для
изготовления сцинтилляц. счетчиков.
===
Исп. литература для статьи «ФЛУОРЕН»: Клар Э., Полициклические
углеводороды, пер. с англ., т. 2, M., 1971, с. 46-52; Ullmann's Encyklopadie,
4 Aufl., Bd 14, Weinheim, 1977, S. 685.
H. H. Артамонова.
Страница «ФЛУОРЕН» подготовлена по материалам химической энциклопедии.
|

