|
ФТАЛЕВЫЙ АНГИДРИД (ангидрид
1,2-бензолдикарбоно-вой к-ты), мол. м. 148,12; бесцв. орторомбич. кристаллы
(параметры решетки а =0,790 HM, b =1,416 HM, с = 0,594
HM); легко возгоняется, т. пл. 130,850C, т. кип. 294,5 0C;
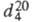 1,527; 1,527;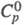 кДж(кг-К): 1,00 (О 0C), 1,07 (20 0C), 1,70 (150 0C);
h (Па-с) 1,19 (133 0C), 0,55 (220 0C); g 0,035
Н/м (155 0C), 0,0327 Н/м (180 0C); давление пара в мм
рт.ст.: 0,0018 (35 0C), 0,11
(5O0C), 0,712 (100 0C), 5,88 (130 0C); DH0обр
-460,02 кДж/моль,
кДж(кг-К): 1,00 (О 0C), 1,07 (20 0C), 1,70 (150 0C);
h (Па-с) 1,19 (133 0C), 0,55 (220 0C); g 0,035
Н/м (155 0C), 0,0327 Н/м (180 0C); давление пара в мм
рт.ст.: 0,0018 (35 0C), 0,11
(5O0C), 0,712 (100 0C), 5,88 (130 0C); DH0обр
-460,02 кДж/моль,
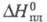 22,93
кДж/моль, DH0сгор -3259
кДж/моль; 22,93
кДж/моль, DH0сгор -3259
кДж/моль; 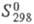 1,79 кДж(моль·°С). Р-римость (в г на 100 г р-рителя): в HCOOH 4,7 (20 0C),
CCl4 0,7 (20 0C), CS2 0,7 (20 0С),
пиридине 80 (25 0C), воде 0,62 (25 0C), 19,0 (100 0C),
95,0 (135 0C; с образованием фталевой к-ты); плохо раств. в этаноле
и диэтиловом эфире.
1,79 кДж(моль·°С). Р-римость (в г на 100 г р-рителя): в HCOOH 4,7 (20 0C),
CCl4 0,7 (20 0C), CS2 0,7 (20 0С),
пиридине 80 (25 0C), воде 0,62 (25 0C), 19,0 (100 0C),
95,0 (135 0C; с образованием фталевой к-ты); плохо раств. в этаноле
и диэтиловом эфире.
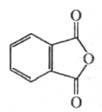
Обладает св-вами ароматических
соединений. При нагр. с моноатомными спиртами в присут. H2SO4
(130-140 0C) или орг. солей Ti (200 0C) образует соответствующие
сложные моно- и диэфиры, с многоатомными спиртами в присут. высоких к-т - полиэфиры
(см. Алкидные смолы). Напр., на основе Ф. а. и диолов (этилен-, диэтиленгликоля,
пропилен-гликоля) получают полиэфиры; на основе Ф. а. и глицерина -алкидные
(глифталевые) смолы.
Хлорирование Ф. а. приводит
к ангидриду тетрахлорфтале-вой к-ты, из к-рого получают самозатухающие полиэфирные
смолы. С PCl5 образует фталоилдихлорид C6H4(COCl)2.
При нитровании Ф. а. дает смесь 3- и 4-нитрофталевых к-т, при сульфировании
- смесь 3- и 4-сульфопроизводных. С NH3 и первичными аминами в зависимости
от условий р-ции Ф. а. образует фталаминовую к-ту (ф-ла I), фталимид (II) или
диамид фталевой к-ты (ПI):
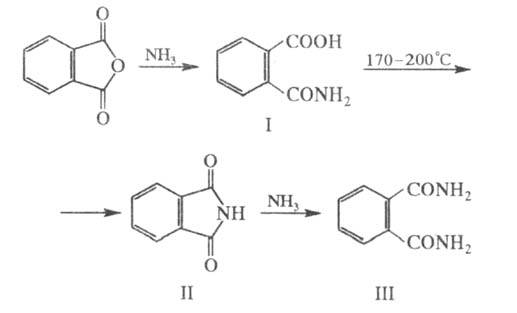
При пропускании паров Ф.
а. и NH3 при 350-400 0C над оксидами Al, V, W, Cr или
Mn получается фталодинитрил.
Конденсация Ф. а. с бензолом
в присут. AlCl3 и H2SO4 приводит к антрахинону:
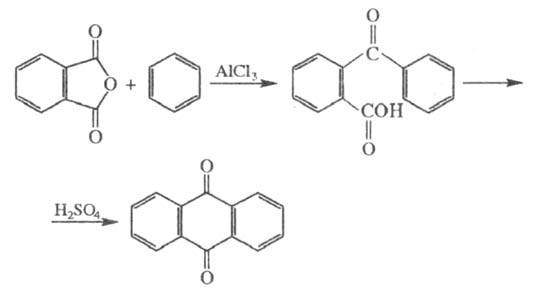
Ф. а. легко реагирует с
фенолами и их производными. Так, р-ция с фенолом в присут. H2SO4
и SnCl2 приводит к фенолфталеину, с м-(этиламино)фенолом
- к родамину, с резорцином - к флуоресцеину (см. Ксантеновые красители),
с n-хлорфенолом - к хинизарину. С мочевиной и солями Cu Ф.
а. образует нерастворимые пигменты фталоцианины, применяемые в качестве
красителей. Декарбоксилирование Ф. а. при 200 0C в присут. Al2O3,
ZnO приводит к бензойной к-те; это один из пром. способов ее получения.
Каталитич. гидрирование
Ф. а. на никелевом катализаторе при 150 0C приводит последовательно
к фталиду, о-толуило-вой к-те, гексагидро-о-толуиловой к-те; гидрирование
при 5 МПа и 300 0C над тем же катализатором - к гексагидро-фталевой
к-те:
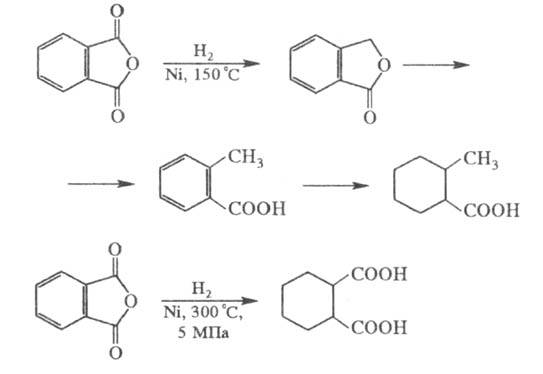
Ф. а. при взаимод. с KOH
превращается в дикалиевую соль фталевой к-ты, к-рая при 350-400 0C
в присут. CaCO3 и Zn изомеризуется в терефталевую к-ту.
В пром-сти Ф. а. получают
парофазным каталитич. окислением кислородом воздуха о-ксилола или нафталина
с использованием стационарных или псевдоожиженных (нафталин) катализаторов на
основе V2O5 - TiO2 или V2O5
- K2SO4. Процесс проводят при 350-400 0C с
избытком O2 воздуха (концентрация
углеводорода 40-80 г/м3). Сырой Ф. а. из реакционных газов улавливают
в твердом виде в аппаратах калориферного типа, очищают и выделяют ректификацией.
Выход при окислении о-ксилола 75-80%, нафталина 85-88%.
Ф. а. применяют в произ-ве
красителей, алкидных смол, пластификаторов, инсектицидов, лек. ср-в, тетрахлорфтале-вого
ангидрида. Ф. а.- реагент для обнаружения и титримет-рич. определения низших
первичных и вторичных алифатич. спиртов, идентификации фенолов и фенольных смол.
Ф. а. токсичен, вызывает
раздражение кожи, слизистых оболочек глаз и носа, способствует заболеванию бронхиальной
астмой. ЛД50 4 г/кг (мыши, перорально); ПДК 1 мг/м3, ПДК
(в воде) 0,5 мг/л. T. всп. 152 0C, т. воспл. 165 0C, т.са-мовоспл.
580-584 0C; КПВ 10,5% по объему. Объем мирового произ-ва ок. 2,5
млн. т в год (1988).
===
Исп. литература для статьи «ФТАЛЕВЫЙ АНГИДРИД»: Гуревич Д.А.,
Фталевый анщдрид, M., 1968; Kirk-Othmer encyclopedia, 3 ed., v. 17, N.Y.,
1982, p. 732-46. А.G. Любарский.
Страница «ФТАЛЕВЫЙ АНГИДРИД» подготовлена по материалам химической энциклопедии.
|

