|
ЦИНКА ОКСИД ZnO, бесцв. кристаллы
гексагон. сингонии (а = 0,32495 нм, с = 0,52069 нм, z
= 2, пространств. группа Р63/тс); т. возг.
1800 °С; плотн. 5,7 г/см3;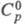 40,28 Дж/ (моль х К);
40,28 Дж/ (моль х К);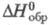 -350,80 кДж/моль,
-350,80 кДж/моль,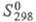 43,67
Дж/(моль х К); показатели преломления 2,015 и 2,068. Амфотерен; с щелочами
дает гидроксоцинкаты, напр., Na[Zn(OH)3], [Na2Zn(OH)4],
[Ba2Zn(OH)6], с р-рами солей - простые или двойные
гидроксосоли Zn(OH)NO3, Zn5(OH)8Cl2
х
2H2O, Zn2Cr(OH)6NO3 x
хН2О, при нагр. с SiO2 и В2О3
- стекловидные Zn2SiO4 и Zn(BO2)2,
с оксидами металлов - цинкаты, напр. CoZnO2. Восстанавливается
до Zn углеродом, СО, Н2, СН4, СаС2 и ферросилицием
при нагр. до ~ 1000 °С. 43,67
Дж/(моль х К); показатели преломления 2,015 и 2,068. Амфотерен; с щелочами
дает гидроксоцинкаты, напр., Na[Zn(OH)3], [Na2Zn(OH)4],
[Ba2Zn(OH)6], с р-рами солей - простые или двойные
гидроксосоли Zn(OH)NO3, Zn5(OH)8Cl2
х
2H2O, Zn2Cr(OH)6NO3 x
хН2О, при нагр. с SiO2 и В2О3
- стекловидные Zn2SiO4 и Zn(BO2)2,
с оксидами металлов - цинкаты, напр. CoZnO2. Восстанавливается
до Zn углеродом, СО, Н2, СН4, СаС2 и ферросилицием
при нагр. до ~ 1000 °С.
Ц. о. встречается в природе в виде минерала
цинкита. Получают Ц. о. обжигом цинкового концентрата, послед. продувкой
его воздухом при 1200 °С и улавливанием пылевидного Ц. о. в спец. фильтрах,
а также сжиганием Zn на воздухе или прокаливанием гидроксида, нитрата или
оксалата Zn. Ц. о.- белый пигмент для красок (цинковые белила), активатор
вулканизации и наполнитель в резиновой пром-сти, компонент косметич. препаратов
- кремов, пудры, лек. ср-в, мазей, паст, присыпок при кожных заболеваниях,
зубных цементов, катализатор синтеза метанола, полупроводниковый материал,
компонент люминофоров.
Ц. о. ядовит, вызывает т. наз. литейную
лихорадку; ПДК в воздухе рабочей зоны 0,5 мг/м3, в атм. воздухе
0,05 мг/м3.
Гидроксид цинка Zn(OH)2 - бесцв.
кристаллы или аморфное в-во; известно 5 полиморфных модификаций Zn(OH)2,
из к-рых устойчивой является только e
(ромбич. сингония); мало раств. в воде, амфотерен (основные св-ва преобладают);
с щелочами образует гидроксоцинкаты, с избытком NH3 - [Zn(NH3)6](OH)2;
получают осаждением щелочами из р-ров солей Zn; применяют для синтеза разл.
соед. цинка.
В. П. Данилов.
===
Исп. литература для статьи «ЦИНКА ОКСИД»: нет данных
Страница «ЦИНКА ОКСИД» подготовлена по материалам химической энциклопедии.
|

