ЭЛЕКТРОДЫ СРАВНЕНИЯ, электрохим. системы, предназначенные для измерения электродных потенциалов. Необходимость их использования обусловлена невозможностью измерения абс. величины потенциала отдельного электрода. В принципе в качестве Э. с. может служить любой электрод в термодинамически равновесном состоянии, удовлетворяющий требованиям воспроизводимости, постоянства во времени всех характеристик и относит, простоты изготовления. Для водных электролитов наиб, часто применяют в качестве Э. с. водородный, каломельный, галогеносеребряные, оксидно-ртутный и хингидронный электроды.
Водородный Э. с. представляет собой кусочек платиновой фольги или сетки, покрытый слоем электролитич. Pt и погруженный частично в р-р, через к-рый пропускают Н2. При адсорбции на электроде образуются адсорбир. атомы Надс. Электродные р-ции на водородном Э. с. описываются ур-ниями: Н2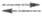 2Надс 2Надс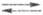 2Н+ + 2е (е - электрон). Водородный электрод при давлении водорода рН2 равном 1 атм (1,01 х 105 Па), термодинамич. активности ионов водорода в р-ре аН+, равной 1, наз. стандартным водородным электродом, а его потенциал условно принимают равным нулю. Потенциалы других электродов, отнесенные к стандартному водородному электроду, составляют шкалу стандартных электродных потенциалов (см. Стандартный потенциал). Дня водородного Э. с. Нернста уравнение записывается в виде: 2Н+ + 2е (е - электрон). Водородный электрод при давлении водорода рН2 равном 1 атм (1,01 х 105 Па), термодинамич. активности ионов водорода в р-ре аН+, равной 1, наз. стандартным водородным электродом, а его потенциал условно принимают равным нулю. Потенциалы других электродов, отнесенные к стандартному водородному электроду, составляют шкалу стандартных электродных потенциалов (см. Стандартный потенциал). Дня водородного Э. с. Нернста уравнение записывается в виде:
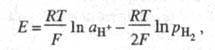
где Т - абс. т-ра; F - постоянная Фарадея; R - газовая постоянная. При рН2 = 1 атм электродный потенциал
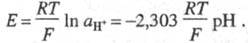
Используется в широком диапазоне рН - от значений, соответствующим конц. к-там, до значений, соответствующим конц. щелочам. Однако в нейтральных р-рах водородный Э. с. может нормально функционировать лишь при условии, что р-р обладает достаточно хорошими буферными св-вами (см. Буферный раствор). Это связано с тем, что при установлении равновесного потенциала на платинированной платине, а также при пропускании тока через водородный Э. с. появляется (или исчезает) нек-рое кол-во ионов Н+, т. е. изменяется рН р-ра, что особенно заметно в нейтральных средах. Водородный электрод применяют в широком интервале т-р, отвечающем существованию водных р-ров. Следует, однако, учитывать, что при повышении т-ры парциальное давление водорода падает вследствие роста давления паров р-рителя и обусловленное этим изменение потенциала Э. с. соответствует ур-нию
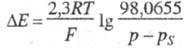 , где р - барометрич. давление (в кПа), a ps - суммарное давление насыщ. паров над р-ром (кПа). Возможность использования водородного электрода в орг. средах требует спец. проверки, т. к. Pt может катализировать процессы с участием орг. соед., вследствие чего нарушается равновесие электродной р-ции и электрод приобретает стационарный потенциал, отличный от равновесного. , где р - барометрич. давление (в кПа), a ps - суммарное давление насыщ. паров над р-ром (кПа). Возможность использования водородного электрода в орг. средах требует спец. проверки, т. к. Pt может катализировать процессы с участием орг. соед., вследствие чего нарушается равновесие электродной р-ции и электрод приобретает стационарный потенциал, отличный от равновесного.
Каломельный Э. с. изготавливают, используя ртуть и р-ры каломели в хлориде калия. Электродная р-ция на этом электроде отвечает ур-нию: 2Hg + 2Сl-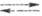 Hg2Cl2, а соответствующее ур-ние Нернста имеет вид: Hg2Cl2, а соответствующее ур-ние Нернста имеет вид:
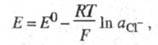
где E0 - стандартный потенциал. В зависимости от концентрации КС1 различают насыщенный, нормальный и децинормальный каломельные Э. с. Эти Э. с. хорошо воспроизводимы, устойчивы и пригодны для работы при т-рах до 80 °С. При более высоких т-рах начинается разложение хлорида ртути. Часто каломельный Э. с. подсоединяют через солевой мостик, состоящий из концентриров. р-ра КС1 для снижения диффузионного потенциала. Потенциал Е каломельного Э. с. зависит от т-ры, причем температурный коэф. минимален для децинормального электрода, для к-рого Е =0,3365 - 6 х 10-5(t-25), где t - т-ра (°С).
Галогеносеребряные Э. с. представляют собой серебряную проволоку, покрытую галогенидом серебра, к-рый наносится путем термич. или электрохим. разложения соли серебра. Электродная р-ция отвечает ур-нию: Ag + Hal-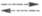 AgHal + е (Hal - галоген), а ур-ние Нернста имеет вид: . AgHal + е (Hal - галоген), а ур-ние Нернста имеет вид: .
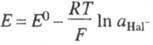
Удобны при работе с электрохим. ячейками без жидкостного мостика, применимы как в водных, так и во мн. неводных средах, устойчивы при повышенных т-рах. В области т-р 0-95 °С потенциал хлорсеребряного Э. с. описывается ур-нием: E=0,23655-- 4,8564 x 10-4t - 3,4205 x 10-6t2 + 5,869 x 10-9t3.
Оксидно-ртутный Э.с. приготавливают из ртути и насыщенных р-ров оксида ртути в водном р-ре щелочи. Электродная р-ция: Hg2O + 2e + H2O 2Hg + 2OH ; 2Hg + 2OH ;
ур-ние Нернста:
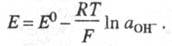
Удобен при работе в щелочных р-рах, т. к. при этом легко реализовать цепи без жидкостного соединения.
Хингидронный Э. с. представляет собой платиновую проволочку, опущенную в насыщ. р-р хингидрона. Электродная р-ция: С6Н4(ОН)2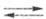 С6Н4О2 + 2Н+ + 2е. Стандартный потенциал E° = 0,6992 В. Используется в интервале рН 0-6, а в буферных р-рах в отсутствие сильных окислителей - до рН С6Н4О2 + 2Н+ + 2е. Стандартный потенциал E° = 0,6992 В. Используется в интервале рН 0-6, а в буферных р-рах в отсутствие сильных окислителей - до рН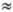 8,5. В интервале т-р 0-50 °С потенциал хингидронного Э. с. выражается ур-нием: Е = 0,6992 - 7,4 x 10-4(t -25) + [0,0591 + 2 x 10-4(t -25)] lgaН+ . 8,5. В интервале т-р 0-50 °С потенциал хингидронного Э. с. выражается ур-нием: Е = 0,6992 - 7,4 x 10-4(t -25) + [0,0591 + 2 x 10-4(t -25)] lgaН+ .
При измерениях в неводных средах в принципе можно применять водные Э. с., если создать воспроизводимую границу водного и неводного р-ров и учитывать возникающий на этой границе диффузионный потенциал. Часто в неводных средах используют Э. с. на основе серебра в р-ре его соли.
В расплавленных солевых системах наиболее часто используются Э. с., основанные на паре AgI/Ag, к-рая стабильна в разл. расплавах.
Потенциалы водных Э. с. по отношению к стандартному водородному электроду при 25 °С приведены в табл.:
|
Электрод |
Потенциал, В |
|
Насыщенный каломельный: Hg | Hg2Cl2, насыщенный КС1 |
0,2412 |
|
Нормальный каломельный: Hg| Hg2Cl2, 1M КС1 |
0,2801 |
|
Децинормальный каломельный: Hg| Hg2Cl2, 0,1M KC1 |
0,3337 |
|
Хлорсеребряный: Ag | AgCl, насыщенный КС1 |
0,197 |
|
Оксидно-ртутный: Hg| HgO, 0.1M NaOH |
0,926 |
Лит.: Справочник по электрохимии, под ред. A.M. Сухотина, Л., 1981; Практикум по электрохимии, под ред. Б. Б. Дамаскина, М., 1991; Ives D. J. G., Janz G. J., Reference electrodes, N. Y., 1961; Minh N. Q., Redey L., в кн.: Molten salt techniques, v. 3, eds. D. C. Loverring, R.J. Gale, N. Y., 1984, p. 105-287.
О.А.Петрий.
|

