ЭРБИЙ (от назв. селения Иттербю, Ytterby в Швеции; лат. Erbium) Еr, хим. элемент III гр. периодич. системы, относится к редкоземельным элементам; ат. н. 68, ат. м. 167,26. В природе 6 стабильных изотопов: 162Еr(0,14%), 1б4Еr(1,61%), 166Еr(33,6%), 167Еr(22,95%), 168Еr(26,8%), 170Еr(14 9%). Конфигурация внеш. электронных оболочек атома 4f l25s25p66s2; степени окисления +3, редко +1; энергии ионизации при последоват. переходе от Ег0 к Еr5+ равны соотв. 6,10, 11,93, 22,74, 42,65, 65,1 эВ; электроотрицательность по Полингу 1,24; атомный радиус 0,175 нм, ионные радиусы Еr3+ (в скобках даны координац. числа) 0,103 (6), 0,109 (7), 0,114 (8), 0,120 (9) нм.
Содержание в земной коре 3,3 x 10-4% по массе, в морской воде 6 x 10-7 мг/л. Вместе с др. РЗЭ содержится в минералах ксенотим, эвксенит, монацит, бастнезит, лопарит, ортит и др.
Свойства. Э.- серебристо-белый металл, имеет одну кристаллич. модификацию структурного типа Mg с гексагон. кристаллич. решеткой, а = 0,35588 нм, с = 0,55874 нм, z = 2, пространств. группа Р63/ттс; т. пл. 1522 °С, т. кип. 2510 °С; плотн. 9,062 г/см3;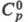 28,12 Дж/(моль х К); 28,12 Дж/(моль х К);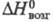 316,5 кДж/ моль; 316,5 кДж/ моль;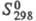 73,18 Дж/(моль х К); давление пара при т-ре плавления 2-8 МПа; температурный коэф. линейного расширения 1,23 х 10-5 К-1; 73,18 Дж/(моль х К); давление пара при т-ре плавления 2-8 МПа; температурный коэф. линейного расширения 1,23 х 10-5 К-1;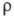 8,5 х 10-7 Ом х м; парамагнетик, магн. восприимчивость +2,63 х 10-7; ферромагнетик ниже 20 К (точка Кюри); антиферромагнетик ниже 84 К (т-ра Нееля); модуль упругости 74,8 ГПа, модуль сдвига 30,2 ГПа; коэф. Пуассона 0,238; 8,5 х 10-7 Ом х м; парамагнетик, магн. восприимчивость +2,63 х 10-7; ферромагнетик ниже 20 К (точка Кюри); антиферромагнетик ниже 84 К (т-ра Нееля); модуль упругости 74,8 ГПа, модуль сдвига 30,2 ГПа; коэф. Пуассона 0,238;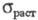 286 МПа. Легко поддается мех. обработке (инертная атмосфера). 286 МПа. Легко поддается мех. обработке (инертная атмосфера).
СВОЙСТВА НЕКОТОРЫХ СОЕДИНЕНИЙ ЭРБИЯ
|
Показатель |
Еr2O3 |
ErF3 |
ErCl3 |
|
|
Цвет |
Светло-розовый |
Светло-розовый |
Розово-фиолетовый |
|
|
Сингония |
Кубич. |
Моноклинная |
Ромбет. |
Тритон. |
Моноклинная |
|
|
Параметры ячейки: а, нм |
|
|
|
|
|
|
|
b,нм |
_ |
0,3470 |
0,6846 |
_ |
1,179 |
|
|
с, нм |
_ |
0,8555 |
0,4380 |
0,4125 |
0,639 |
|
|
угол, град |
_ |
100,17 |
_ |
_ |
110,7 |
|
|
Число формульных единиц в ячейке |
16 |
6 |
4 |
1 |
4 |
|
|
Пространственная группа |
Ia3 |
C2/m |
C3m1 |
C3ml |
С2/m |
|
|
Т. пл., °С |
2380 |
1020a (3 МПа) |
1117a |
1146 |
776 |
|
|
Т. кип., °С |
<3500 |
_ |
_ |
_ |
1500 |
|
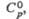 Дж/(моль x К) Дж/(моль x К) |
108,5 |
— |
100,8 |
— |
— |
|
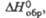 кДж/моль кДж/моль |
-1897,86 |
— |
-1698 |
29,5б |
-1000,3 |
|
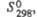 Дж/(моль х К) Дж/(моль х К) |
154,3 |
— |
121,3 |
— |
155 |
|
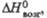 кДж/моль кДж/моль |
— |
— |
462,3 |
— |
280,9 |
|
а Т-ра полиморфного перехода.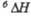 полиморфного перехода. полиморфного перехода.
На воздухе компактный Э. окисляется медленно, при нагр. во влажном воздухе неск. быстрее, с минеральными к-тами дает соли, кипящей водой медленно окисляется, взаимод. с О2, галогенами, халькогенами, N2 и Н2 при натр., давая соед. Еr(III). В водных средах Э. существует в виде гидратир. ионов Еr3+ . С разл. орг. и неорг. лигандами ион Еr(III) образует соед. с координац. числами от 9 до 15. По хим. св-вам подобен др. лантаноидам(III). Еr(I) известен только в гидролитически неустойчивых галогенидных кластерах типа ЕrХ, Еr4Х5, Еr7Х10, Еr6Х7 и т. п., где X = С1, Вr, I, образующихся при взаимод. металлич. Э. с ЕrХ3. Соед. Еr(III) окрашены в розовый цвет, моногалогениды имеют черную окраску.
Сесквиоксид Еr2О3 (табл.) получают разложением Er(NO3)3, Er2(SO4)3, Er2(CrO4)3, или др. солей на воздухе обычно при 800-1000 °С; компонент спец. керамик, люминофоров, лазерных стекол; временно допустимая концентрация в воздухе 4 мг/м3.
Трифторид ErF3 получают взаимод. Еr2О3 с HF-газом при 500 °С, термич. разложением фгораммониевых солей, напр. (NH4)3ErF6, при 400-500 °С в атмосфере Аr, N2; применяют для получения чистого металлич. Э. металлотермич. способом, в качестве компонента твердых электролитов. Трихлорид ЕrС13 сильно гигроскопичен; получают взаимод. смеси С12 и СС14 с оксидом или оксалатом Э. выше 200 °С, хлорированием Э. и др.; применяют для получения металлоорг. соед. Э. и металлич. Э. металлотермически или электрохимически.
Получение и применение. Э. из прир. смеси РЗЭ выделяют методами экстракции и хроматографии. Дальнейшую очистку, как правило, проводят хроматографически. Металлич. Э. получают из фторида и хлорида металлотермически или электрохимически. Выпускают в небольших масштабах и используют гл. обр. в исследоват. целях как активатор люминесценции (в т. ч. в твердотельных лазерах), для изготовления магн. материалов (сплавы с Fe, Co, Ni, Re).
Э. был открыт К. Мосандером при исследовании эрбиевых концентратов в 1843.
Комплексные соединения Э. характеризуются чаще всего высокими координац. числами (вплоть до 12), что обусловлено большими размерами ионов Ег(Ш). Для координац. соед. Э. известны октаэдрические, пентагонально-бипирамидальные, додеказдрические, икосаздрические, призматические и др. координац. полиэдры. Хим. связь эрбий-лиганд преим. ионная, эффективные заряды на атоме Э. в соед. от +2,5 до +2,7, т. е. имеется нек-рый вклад ковалентной составляющей. Ковалентность увеличивается в ряду РЗЭ по мере уменьшения размера ионов РЗЭ(III) и для Э. существенно более значима по сравнению с легкими РЗЭ (лантаном, неодимом).
Комплексные соед. Э. имеют относительно высокие константы устойчивости, что в особенности характерно для соед. с полидентатными лигандами. Из неорг. производных наиб. важны гидроксокомплексы состава [Еr(Н2О)т(ОН)п]3-n, где n =1-3, т = 2-6, галогенидные комплексы, как катионные (напр., состава [МХ]2+), так и анионные (напр., [МХ4]-,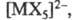 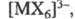 где X - галоген), нитратные, сульфатные, фосфатные и т. д. Стабильность ацидокомплексов уменьшается в след, ряду лигандов: где X - галоген), нитратные, сульфатные, фосфатные и т. д. Стабильность ацидокомплексов уменьшается в след, ряду лигандов:
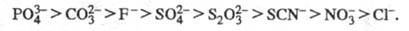
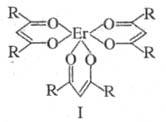
Из комплексов с орг. лигандами перспективны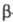 -дикетонаты, используемые для группового разделения РЗЭ путем фракционной сублимации. В этих случаях чаще всего применяют дипивалоилметанаты [ф-ла I, R = (СН3)3С] или ацетилацетонаты (I; R = СН3). Используются, кроме того, комплексы с дикарбоновыми к-тами (оксалаты, малонаты, сукцинаты и др.), монокар-боновыми к-тами (вплоть до С30), с аминами, а также комплексонаты. -дикетонаты, используемые для группового разделения РЗЭ путем фракционной сублимации. В этих случаях чаще всего применяют дипивалоилметанаты [ф-ла I, R = (СН3)3С] или ацетилацетонаты (I; R = СН3). Используются, кроме того, комплексы с дикарбоновыми к-тами (оксалаты, малонаты, сукцинаты и др.), монокар-боновыми к-тами (вплоть до С30), с аминами, а также комплексонаты.
Последние применяют в технологии разделения и глубокой очистки РЗЭ методами ионного обмена, экстракции. Получают комплексные соед. Э. (как и других РЗЭ) взаи-мод. оксидов, гидроксидов, а также р-ров солей Еr(III) с соответствующими лигандами с послед. кристаллизацией при упаривании р-ра или высаливании из него. Применяют их в технологии разделения и очистки собственно РЗЭ, при отделении лантаноидов и актиноидов и др. Чаще всего эти соед. в технол. практике являются полупродуктами при получении разнообразных материалов, в т. ч. галогенидных, оксидных и др. стекол, керамик со св-вами высокотемпературных сверхпроводников и др.
Химия других, по крайней мере тяжелых, РЗЭ подобна химии комплексных соед. Э.
Л. И. Мартыненко. Ю. М. Киселев, С. Д. Моисеев.
|

