|
БОРНЫЕ КИСЛОТЫ. Ортоборная к-та (борная к-та) Н3ВО3
- бесцв. кристаллы, решетка слоистая, триклинная (а = Ь =
0,704 нм, с = 0,656 нм,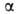 =
101,10°, =
101,10°,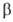 = 92,30°,
= 92,30°,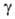 =
= 120,00°, z = 4, пространств. группа Рl, расстояния между слоями 0,318
нм); плотн. 1,46 г/см3. При давлении выше 4200 МПа образуется
модификация с ромбич. решеткой, выше 5700 МПа - с тетрагональной. При медленном
нагревании Н3ВО3 при 107,5°С превращается в метаборную
к-ту НВО2, при 160°С - в В2О3. Т. пл.
170,9°С (с разл.); Сoр 81,3 Дж/(моль*К); =
= 120,00°, z = 4, пространств. группа Рl, расстояния между слоями 0,318
нм); плотн. 1,46 г/см3. При давлении выше 4200 МПа образуется
модификация с ромбич. решеткой, выше 5700 МПа - с тетрагональной. При медленном
нагревании Н3ВО3 при 107,5°С превращается в метаборную
к-ту НВО2, при 160°С - в В2О3. Т. пл.
170,9°С (с разл.); Сoр 81,3 Дж/(моль*К);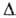 Hoпл
22,34 кДж/моль, Hoпл
22,34 кДж/моль, Hoисп
98,1 кДж/моль, Hoисп
98,1 кДж/моль,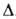 Hoвозг
63,97 кДж/моль, Hoвозг
63,97 кДж/моль,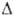 Hoобр
- 1094,9 кДж/моль; Sо298 88,74 Дж/(моль*К).
Раств. в воде (2,60% по массе при 0°С, 4,80% при 20°С, 10,35% при 50°С,
28,7% при 100°С), глицерине (19,48% при 25°С), метаноле (21,0%), этаноле
(11,2%), ацетоне (0,65%), жидком NH3, диоксане, пиридине; практически
не раств. в эфире. Hoобр
- 1094,9 кДж/моль; Sо298 88,74 Дж/(моль*К).
Раств. в воде (2,60% по массе при 0°С, 4,80% при 20°С, 10,35% при 50°С,
28,7% при 100°С), глицерине (19,48% при 25°С), метаноле (21,0%), этаноле
(11,2%), ацетоне (0,65%), жидком NH3, диоксане, пиридине; практически
не раств. в эфире.
Б.к. - слабая к-та; Ka1 = 5,8*10-10, Ka2
= 4*10-13, Ka3 = = 4*10-14.
Кислотные св-ва в водном р-ре обусловлены образованием Н+ по
р-ции: Н3ВО3 + Н2О -> [В(ОН)4]-+
Н+ . По мере увеличения концентрации Н3ВО3
в р-ре образуются полиборатные анионы, напр. [В3О3(ОН)4]-,
[В4О5(ОН)4]2-. Со спиртами
и полиолами Н3ВО3 в присут. H2SO4
образует эфиры, в присут. щелочей - комплексные соединения.
В природе Н3ВО3 встречается в виде минерала сассолина,
а также в термальных водах и прир. рассолах, из к-рых ее экстрагируют спиртами
или смесью полиолов либо сорбируют неорг. и орг. сорбентами. При получении
Н3ВО3 из прир. боратов их разлагают H2SO4
при 100°С и отфильтровывают нерастворимый остаток; фильтрат охлаждают до
15°С, выпавшие при этом кристаллы Н3ВО3 отделяют
на центрифугах и сушат при т-ре не выше 100°С. Используют для получения
спец. стекла, эмалей, цементов, флюсов, моющих и косметич. ср-в, огнезащитных
составов, как дезинфицирующее и консервирующее ср-во, ингибитор коррозии,
реагент в фотографии, в кач-ве микроудобрения, в произ-ве др. борсодержащих
соединений. Объемы произ-ва Н3ВО3 в основных странах-производителях
в 1981: в США - 300, Турции - 150 тыс. т/год. ПДК в сточных водах санитарно
- бытового назначения 0,5 мг/л (в пересчете на В).
Б.к. впервые была получена из буры в 1702 В. Гомбергом.
Мета борная к-та НВО2 - бесцв. кристаллы. Существует в трех
модификациях: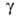 (наиб.
устойчива) с кубич. решеткой (а = 0,887 нм, z = 24), т. пл. 236
°С (с разл.), плотн. 2,486 г/см3, (наиб.
устойчива) с кубич. решеткой (а = 0,887 нм, z = 24), т. пл. 236
°С (с разл.), плотн. 2,486 г/см3, Нообр
-804,6 кДж/моль; Нообр
-804,6 кДж/моль;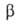 с моноклинной решеткой, т. пл. 200,9 °С (с разл.), плотн. 2,045 г/см3,
с моноклинной решеткой, т. пл. 200,9 °С (с разл.), плотн. 2,045 г/см3,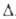 Нообр
— 794 кДж/моль; Нообр
— 794 кДж/моль;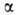 с ромбич. решеткой, т. пл. 176°С (с разл.), плотн. 1,784 г/см3,
с ромбич. решеткой, т. пл. 176°С (с разл.), плотн. 1,784 г/см3,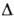 Нообр
- 789,3 кДж/моль. Т-ра перехода Нообр
- 789,3 кДж/моль. Т-ра перехода 160°С. С водой НВО2 легко образует Н3ВО3.
160°С. С водой НВО2 легко образует Н3ВО3.
В водных р-рах предполагается существование полиборных к-т общей ф-лы
Н3m_2nВmО3m_n.
===
Исп. литература для статьи «БОРНЫЕ КИСЛОТЫ»: ТкачевК. В., Плышевский Ю. С, Технология неорганических
соединений бора, Л, 1983. Г.Н. Кононова.
Страница «БОРНЫЕ КИСЛОТЫ» подготовлена по материалам химической энциклопедии.
|

