Размеры молекулы рассчитаны с помощью пакета программ ChemiSiteSW. Для протекания реакции, необходимо, чтобы физически реализовались, кроме необходимых условий (насыщение химических связей), еще и достаточные стерические пространственные условия. Активные участки реагирующих молекул должны пространственно совпасть молекула реагента должна не только «догнать» партнера, но еще и «повернуться» к ней активной стороной. Поэтому следует ожидать достаточно четкую корреляцию процесса и от частоты вращения молекул – величины, обратно пропорциональной корню квадратному из момента инерции молекулы (М-0,5Rg1). Действительно, как показал анализ, что таковая наблюдается с коэффициентом корреляции равным 0,862.
Для рассмотренного ряда аминов это не удивительно, но это окажется очень важным обстоятельством при рассмотрении диаминов. Рассмотренные выше корреляции показывают, что наиболее активными аминами проявляют себя амины, обладающие наиболее высокими отрицательными зарядами на атомах азота или, соответственно, положительными на аминном протоне. Поэтому, чтобы выяснить какие водородные связи реально участвуют в процессе, имеет смысл провести корреляцию и с учетом этих зарядов. На рис. 4 показаны результаты проведенной корреляции приращения ОЧ от времени контакта, умноженной на величину заряда на аминном протоне. Аналогичный анализ был проведен и для заряда на азоте. Здесь также наблюдалась вполне хорошая корреляция с коэффициентом равным 0,918. Сравнение корреляций позволяет сделать вывод о том, что, по-видимому, для этого ряда аминов существенными являются водородные связи, возникающие между протонами амина и атомами кислорода перекисей. Что касается последовательности расположения добавок в ряду толуидинов (3 , 4, 5 см. табл. 1), то она просто объясняется устойчивостью вращения молекулы вокруг главной оси инерции, что прямо связано с величиной момента инерции молекулы J =2/5 M•Rg2 (момент инерции шара). 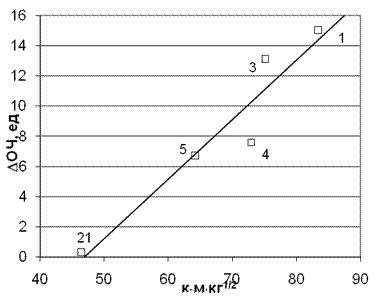
Рис. 4. Корреляция приращения ОЧ от произведения заряда на аминном протоне на время молекулярного контакта для радикала С2Н5ОО• с молекулярной массой М0 =61 (точки на графике соответствуют номерам аминов в табл. 1). Коэффициент корреляции К = 0,969. Чем больше момент инерции, тем устойчивее в пространстве движение молекулы. Среди изомеров толуидина по величине радиуса Rg (см. табл. 1) орто изомер (3), в силу своей малой симметрии структуры, движется в пространстве совершенно беспорядочно. Аналогичная ситуация возникает и в ряду ксилидинов (см. рис. 5). Сравнение корреляций позволяет сделать вывод о том, что, по-видимому, для этого ряда аминов существенными являются водородные связи, возникающие между протонами амина и атомами кислорода перекисей. Топлива группы I (с ОЧИ 86-91) также были проверены на аналогичные корреляции, и для этой довольно большой группы аминов подтвердилась ожидаемая корреляция. Из особенностей изученной группы аминов отметим, во-первых, то, что для топлив с таким высоким значением ОЧ наблюдаются относительно малые значение приращения ОЧ, как это и понятно из предлагаемого механизма. Далее, если для топлив II группы анализировались моноамины, то в данном случае сравнительному анализу подверглись наряду с ними и диамины. Последние естественно более активны, чем моноамины, но и они хорошо укладываются в предлагаемую корреляцию. В данную группу попали амины с довольно широким спектром молекулярных масс и скоростей теплового движения молекул. По отработанной методике, рассмотренной выше, проводилась также серия корреляций приращения ОЧ: - от молекулярной массы М (с коэффициентом корреляции равным 0,271);
- от скорости теплового движения (от массы М 0,5) с коэффициентом корреляции равным 0,213. Однако, с переходом к дальнейшим корреляциям, учитывающим:
- относительную скорость движения (с коэффициентом корреляции равным 0,213);
- время контакта (с коэффициентом корреляции равным 0,233);
- произведения времени контакта на заряд аминного протона (рис. 4) (с коэффициентом корреляции равным 0,797);
происходит существенное улучшение корреляции. Корреляция ухудшается, если перейти к учету заряда на атоме азота. Это обстоятельство снова подтверждает утверждение о том, что главную роль в связывании «вредных» радикалов в предпламенных процессах играют водородные связи, возникающие между протонами амина и кислородными атомами перекисей. Соображения симметрии в ряду ксилидинов определяют их взаимное расположение по эффективности. Здесь ситуация совершенно аналогичная той, что мы имели в случае толуидинов. Действительно, моменты инерции этих изомеров убывают в последовательности убывания их в ряду мета пара орто- (см. табл. 1). Эти свойства симметрии молекул аминов и определяют их расположение по величине приращения ОЧ. Приведенная корреляция на рис. 4 показывает, что амины с большим зарядом на протоне сравнительно более эффективны. Казалось бы, это правило нарушают диамины, которые успешно конкурируют в этом отношении, хотя и имеют гораздо меньший заряд. 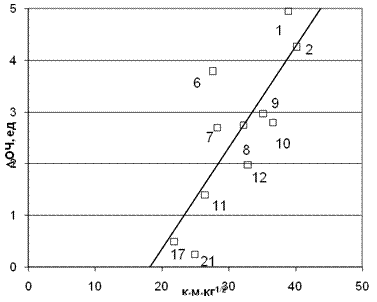
Рис. 5. Корреляция между приращением ОЧ и произведением заряда на аминном протоне на время молекулярного контакта (Мо=48). Коэффициент корреляции 0,818.
(Если писать 42, то надо говорить о сумме Мо1 и Мо2) Это противоречие легко устраняется, если учесть стерический фактор. Чтобы прореагировать, реагенту необходимо занять соответствующее пространственное положение по отношению к партнеру, т.е. молекуле нужно повернуться. Корреляция, приведенная ниже, как раз и относится к такому случаю. Скорость поворота молекулы или частота ее вращения пропорциональна корню квадратному из ее момента инерции, поэтому для таких симметричных молекул, как диамины, вполне справедливо утверждение, что для вступления в реакцию им достаточно повернуться не на полный оборот, а совершить лишь пол-оборота. Это или увеличивает формально их частоту вращения в 2 раза, что фактически увеличит время контакта в корень из 2 раз, или, наконец, увеличит заряд в корень из 2 раз. Изложенное обстоятельство и должно объяснить аномальную «рокировку» диаминов, что показано на рис. 6, где корректировка частоты вращения молекул диаминов резко улучшила коэффициент корреляции до значения 0,887. Более того, если из массива аминов исключить несимметричную молекулу ортоксилидина (12), то корреляция резко улучшиться до значения коэффициента корреляции равного 0,95.
|
