
Катализом называют процесс изменения скорости химической реакции под влиянием веществ, которые в ходе реакции не изменяют своего состава. При производстве полимеров и полимерных материалов катализ является очень важным процессом. При этом проблема ускорения реакций полимеризации заключается не только в подборе того или иного катализатора, но и в том, чтобы выбранный катализатор, остающийся в полимере после реакции, не ухудшал его эксплутационные свойства.
Композиции для получения полиуретанов содержат изоцианаты, гидроксилсодержащие олигомеры, а в некоторых случаях наполнители, красители и антипирены. В их производстве широко используются катализаторы. Чрезвычайно важной становится роль катализатора для получения пенополиуретанов, в композицию которых в качестве газообразователя входит вода и эмульгаторы. «Ускорители»
В качестве катализаторов наиболее часто применяют три группы соединений: третичные амины, металлоорганические соединения и соли металлов. К настоящему времени также известны сотни соединений и систем (комбинаций из нескольких соединений, чаще двух компонентов), обладающих в той или иной степени каталитической активностью в реакциях получения уретана.
Основа всех каталитических механизмов синтеза уретана — комплексообразование катализаторов с реагентами. Очень важно иметь точные знания о механизме реакции, поскольку только в этом случае можно обоснованно проводить поиск оптимального катализатора.
Третичные амины служат катализаторами для реакций взаимодействия изоцианатов с гидроксилсодержащими соединениями и водой. Эффективность этих катализаторов возрастает по мере увеличения основности амина и уменьшения пространственных препятствий (табл. 1). | Таблица 1. Сопоставление константы каталитической реакции уретанообразования kк с основностью kв 20 третичных аминов | | Амины | kв 20 | kк | | | Хиноламин | 6,3х10-10 | 0,29 | | | Пиридин | 2,3х10-9 | 0,56 | | | α-Пиколин | 3х10-8 | 0,61 | | | Триэтиламин | 5,65х10-4 | 7,45 | |
Обращаем внимание на низкую величину стерической характеристики EN = 1,3 для катализатора DABCO. Этот амин является дитретичным основанием, где атомы азота связаны тремя мостиками -CH2CH2-. Благодаря такому строению этот катализатор обладает высокой каталитической активностью в реакциях уретанообразования.
Оловоорганические соединения являются очень эффективными катализаторами реакции ОН-содержащих соединений c изоцианатами, в то же время реакцию вода — изоцианат они ускоряют менее эффективно.
При использовании соединений двухвалентного олова (олеат олова, октоат олова, соли бутилолова, каприлат олова и др.) реакция протекает через стадию образования каталитического комплекса из соединения олова и спирта.
Оловоорганические катализаторы в реакциях на основе сложных полиэфиров используются незначительно. Дело в том, что даже самый распространенный оловоорганический катализатор — октоат олова — легко подвергается гидролизу и окислению, что не позволяет добавлять его в полиольные компоненты, содержащие воду; в таких смесях более стабильны соединения четырехвалентного олова. Соединения четырехвалентного олова катализируют реакцию взаимодействия спиртов с изоцианатами, протекающую через стадию образования каталитических комплексов со спиртом или тройных комплексов спирт — катализатор — изоцианат.
Найдена экстремальная зависимость логарифма каталитической константы скорости уретанобразования от логарифма константы устойчивости комплексов соединений Sn(IV) как катализаторов (рис. 3).
Большое число работ посвящено изучению реакций гидроксилсодержащих соединений с изоцианатами при совместном использовании третичных аминов и оловорганических соединений. Одним из важных аспектов в кинетике уретанообразования является синергический эффект, наблюдаемый при этом (табл. 2), механизм которого объясняется образованием каталитически активных центров в комплексах третичных аминов с оловоорганическим соединением.
| Таблица 2. Относительная активность катализаторов | | Катализатор | Концентрация г/100 г | Относительная активность | | | DABCO | 0,1 | 130 | | | DABCO | 0,2 | 260 | | | DABCO | 0,3 | 330 | | | Дибутилоловодилаурат | 0,1 | 210 | | | Дибутилоловодилаурат | 0,5 | 670 | | | Каприлат олова (2+) | 0,1 | 540 | | | Каприлат олова (2+) | 0,3 | 3500 | | | DABCO + дибутилоловодилаурат | 0,2+ 0,1 | 1000 | | | DABCO + каприлат олова (2+) | 0,3+ 0,3 | 4250 | |
К третьей группе катализаторов можно отнести гидроокиси и алкоголяты щелочных металлов, щелочные соли карбоновых кислот, соединения свинца, сурьмы, цинка, меди, кобальта, ацетилацетонаты и другие хелатные комплексы металлов.
Все шире используются пенополиуретаны на основе продуктов полициклоприсоединения и декарбонилирования диизоцианатов. В их основе лежат реакции тримеризации изоцианатов и образования карбодиимидов.
За счет этих реакций формируются изоцианураты и карбодиимиды, обладающие высокой термостабильностью до 400оС и огнестойкостью, которая обеспечивается сшитыми структурами.
В этих системах пены образуются при физическом вспенивании (за счет низкокипящих фреонов).
Выбор каталитической системы Как это «по-химически» | | При взаимодействии диизоцианатов с гидроксилсодержащими олигомерами образуются макродиизоцианаты с уретановыми звеньями (рис. 1). При избытке изоцианата в реакционной среде на концах растущих макромолекул оказываются изоцианатные (— NCO) группы, которые могут вступать в реакции с водой (рис. 2). При этом выделяется углекислый газ, вспенивающий композицию, а макромолекулы полимера присоединяются друг к другу через карбамидные группы. Взаимодействие изоцианатных групп с гидроксилсодержащими олигомерами и с водой — конкурирующие реакции, в которых роль катализатора сводится к регулированию их скорости. При этом выделение газа и рост полимерных молекул должны происходить с такими скоростями, чтобы газ оставался в полимере, а образовавшаяся пена была бы достаточно прочной и не «опадала». |
| Рис. 1. Схема реакции диизоцианатов с гидроксилсодержащими олигомерами | 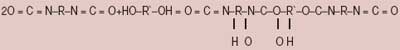 | | Рис. 2 Схема взаимодействия макродиизоцианата с водой | 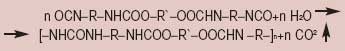 |
Основной проблемой практического осуществления процесса циклической тримеризации изоцианатов, представляющего интерес при получении жестких и эластичных полиуретанизоциануратов, является подбор каталитических систем, избирательно ведущих уретанобразования и циклотримеризацию.
В настоящее время предложено большое число соединений, ускоряющих реакции циклотримеризации изоцианатов:
• амины R3N, RIRIIRIIIN;
• фосфины и фосфиты;
• основания P, As, Sb, четвертичные аммониевые основания, их алкоголяты и карбоксилаты;
• алкоксиды и оксиды металлов;
• карбоксилаты R– COOM, M = Na, Ca, Fe, Mg, Hg, Ni, Co, Zn, Cr, Al, Sn, V, Ti;
• металлоорганика, металлы: Zn, Si, Sn, Pb, Co;
• комбинированные каталитические системы;
• кислоты;
• сульфониевые цвиттер-ионы;
• этиленоксид;
• гидриды.
Циклотримеризация осуществляется путем миграционной полимеризации изоцианатов через взаимодействие с протонодонарами, включающими внедрение RNCO по активированной связи протонодонара R–H, с образованием уретана, аллофаната, предтримера, тримера. При этом решающую роль в селективности каталитической системы играет конформационный контроль на каждой элементарной стадии присоединения.
Карбодиимиды получают каталитическим декарбонилированием изоцианатов. В качестве катализаторов также предлагается большое количество соединений, из которых наиболее активны замещенные фосфорциклопентены: фосфолины (I), их ненасыщенные аналоги — фосфолидины (II), а также окиси и сульфиды фосфолинов (III) и фосфолидинов (IV):
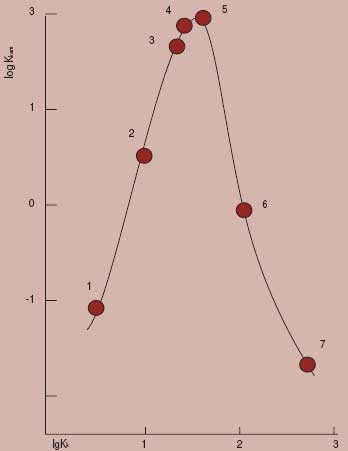 | | Рис. 3 Зависимость активности Sn-органических катализаторов от устойчивости их комплексов со спиртом:1 — (C2H5)4 Sn, 2 — (C2H5)3 SnCl, 3 — (C2H5)2 SnCl2,4 — (C4H9) Sn (OOCCH3)2, 5 — (C4H9)2 Sn (OOCC11H23)2,6 — (C2H5) SnCl3, 7 — SnCl4 . |
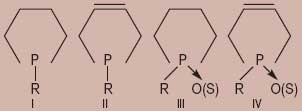
Интерес к каталитическому процессу образования карбодиимидов и получения пенополимеров на их основе растет, что приведет к прогрессу в этой области химии.
Рассматривая катализ превращений изоцианатов в уретаны, изоцианураты, карбодиимиды, мы касались широко апробированного введения катализаторов в реакционную систему как отдельного компонента этой системы.
Новые пути катализа
Есть еще один путь ускорения превращений изоцианатов. Речь идет о катализе иммобилизованными комплексами. Этот путь может быть реализован в процессе наполнения пенополиуретанов, который приводит к упрочнению газонаполненного материала. Для наполнения пенопластов пригодны те же наполнители, что и для монолитных пластмасс: дисперсные, волокнистые, объемные. Проблема заключается в том, что предварительно наполнитель следует обработать катализатором, иммобилизировать катализатор на поверхность наполнителя.
Была также изучена реакция уретанобразования в присутствии оловосодержащего полимерного катализатора на основе сополимера малеинового ангидрида со стиролом. Отмечена высокая каталитическая активность полимерного катализатора. Аналогичный результат дает обработка наполнителя аминными катализаторами или соединениями титана, комплексами Cu(2+). Перспективность такого пути подтверждается уже достигнутыми успехами. В заключение хочется коротко остановиться на вопросе влияния катализатора на свойства полиуретановых материалов.
Понятно, что одностадийный способ синтеза пенополиуретанов более рационален в технологическом отношении. Однако в случае многокомпонентных систем не всегда удается реализовать такой же уровень стабильности, который достигается при более направленном двухстадийном синтезе, так как в системах, состоящих из нескольких гидроксилсодержащих соединений, одновременное нахождение в сфере реакции с изоцианатом конкурирующих друг с другом реагентов способствует более случайному распределению их по цепи. Это приводит к получению полимеров с менее регулярной сеткой и к худшим возможностям для межмолекулярных взаимодействий и формирования сетки физических связей, роль которых в полиуретанах велика.
Становится понятным, что для подобных систем вопрос стабильности свойств полимерного материала может быть успешно решен путем выбора подходящего катализатора для регулирования реакционной способности изоцианатов и гидроксилсодержащих соединений в благоприятном направлении.
Дополнительная информация:
1. Саундерс Дж. Х., Фриш К.К. Химия полиуретанов. — М.: Химия, 1968, с. 470.
2. Фаркас А., Миллс Г. Каталитические эффекты в реакциях изоцианатов // Катализ. Полифункциональные катализаторы и сложные реакции. М. Мир, 1965, с. 281–342.
3. Белова Н.А., Богатков С.В., Медведь С.С. Влияние третичных аминов на реакции образования уретанов // Журн. орг. химии, 1982, т. 18, вып. 10, с. 2121–2127.
4. Берлин А.А., Шутов Ф.А. Пенополимеры на основе реакционноспособных олигомеров. М. Химия, 1978, с. 296.
5. Zygmant Wirpsza. Polyurethanes. N.Y.: Ells Horwood Limited, 1993, с. 517.
6. Lipatova T.E., Nizelskii Yu.N. Coordination Catalysis in Reaction of Polyad-dition // Advances in Urethane Science and Technology, 1981, V. 8, chapter 12, c. 217–243.
7. Козак Н.В., Низельский Ю.Н. Проблемы катализа и механизма циклотримеризации изоцианатов под действием каталитической системы амин–эпоксид // Композиционные полимерные материалы. 1996, вып. 57, с. 13–18.
8. Погасян Г.М., Панкратов В.А., Заплишный В.Н., Мацоян С.Г. Политриазины. — Ереван: Изд-во АН Арм.ССР, 1987, с. 615.
9. Reymure H.E., Carletone P.S., Kolacowski R.A., Sayigh A.A. // J. Cell. Plast. — 1975, V. 11, 6, с. 328–344.
10. Frich K.C., Patel K.J., Marsch R.D. // J. Cell. Plast. — 1970, V.6, 5, c. 203–214.
11. Frich K.C., Wong S.-W. // Cell. Polym. — 1989. — V. 8, 6, c. 433–440.
12. Behrendt G., Joel D. Zur katalyse von urethan-isocyanurat polymeren // Plaste und Kautsch. — 1976.– Bd. 23, 3, с. 177–180.
13. Kresta J.E, Shen S., Chen R., Frisch K. C. // Macromol. Chem. — 1977 — V. 178, 8, с. 2495–2498.
14. Красуский Л.А., Мовсум-Заде М. // Журн. Общ. Химии. — 1936 — Т. 8, № 9, с. 1203–1207.
15. Kresta J.E., Frisch K.C. // J. Cell. Plast. — 1975 — V. 11, № 2, с. 1–8.
16. Царфин М.Я. Каталитические системы на основе алкоголятов и карбоксилатов четвертичного аммониевого основания для получения изоциануратсодержащих пенопластов // Автореферат диссертации. канд. хим. наук. Дзержинск 1991, с. 25.
Автор: Ю.Н. Низельский, д.х.н.,
Источник: Полимеры-Деньги
|
