НОРМАТИВЫ СОДЕРЖАНИЯ ХИМИЧЕСКИХ ВЕЩЕСТВ В ВОДОЕМАХ (Часть II)
МЕТОДИЧЕСКИЕ УКАЗАНИЯ МУ 2.1.5.720-98. Утверждены главным государственным санитарным врачом Российской Федерации Г.Г.ОНИЩЕНКО 15 октября 1998 года

6. Определение пороговых концентраций по влиянию веществ на органолептические свойства воды
Органолептические свойства воды - воспринимаемая рецепторами человека совокупность показателей качества воды: запах, привкус, окраска, прозрачность (мутность), наличие пленок или пены на поверхности воды, посторонних включений, плавающих примесей, осадка. Многие вредные вещества способны изменять органолептические свойства воды, поэтому более чем для половины изученных веществ эти свойства были определяющими при установлении их ПДК в воде.
Целью изучения влияния веществ на органолептические свойства воды является установление пороговых концентраций (ПКорг.) по этому признаку вредности с использованием различных методов: полуколичественных - для оценки интенсивности восприятия запаха (привкуса) в баллах и более объективных количественных на основе альтернативных оценок.
6.1. Объем исследований зависит от свойств вещества. Если по результатам полуколичественной оценки вещество или продукты его трансформации незначительно изменяют органолептические свойства воды, и можно предположить, что органолептический признак вредности не будет лимитирующим в установлении величины ПДК, нет необходимости переходить к количественным методам оценки. Если влияние на один из органолептических показателей заведомо более выражено, необязательно оценивать количественно другие показатели органолептической активности. Оценка запаха с провоцированием хлорирования необходима только в том случае, когда строение и свойства вещества позволяют предположить способность к образованию хлорпроизводных соединений. При образовании продуктов трансформации, не нормированных ранее и обладающих более выраженным, чем исходное вещество, влиянием на органолептические свойства воды, проводятся самостоятельные эксперименты по установлению для них пороговых концентраций по органолептическому признаку вредности.
Оценка интенсивности изменений органолептических свойств осуществляется людьми (дегустаторами), предпочтительно специалистами, имеющими опыт в данной области, нежелательно участие курящих лиц.
В эксперименте используются только безопасные для здоровья человека концентрации, которые выбираются по литературным данным или результатам собственных исследований.
При проведении исследований необходимо соблюдение ряда условий, обеспечивающих получение более объективных данных. Помещение должно быть хорошо проветрено, без посторонних запахов. Дегустаторы допускаются к оценке воды через 1,5 - 2 часа после приема пищи, воды.
Предварительно они должны быть ознакомлены с характером запаха и привкуса исследуемой воды. Характер запаха определяется при температуре 20 и 60 град. C, привкуса - при 20 и 40 град. C.
6.2. Для определения запаха воды используются широкогорлые с притертыми пробками колбы Эрленмейера объемом 500 мл, в которые наливают по 200 мл исследуемого образца. В качестве контрольной используется колодезная, ключевая или дехлорированная водопроводная вода, не имеющая не свойственного ей запаха (привкуса).
Колбу с 200 мл исследуемого образца закрывают пробкой и перемешивают ее содержимое вращательными движениями, после чего колба открывается и дегустатор делает несколько глубоких вдохов, определяя характер и интенсивность запаха.
Запах характеризуется качественно в зависимости от его вида, например, ароматический, нефтепродуктов, гнилостный, землистый и др.
6.2.1. Оценка запаха при 60 град. C проводится следующим образом. Горлышко колбы закрывается стеклом и колба подогревается на водяной бане до нужной температуры, после чего анализируется интенсивность запаха.
6.3. Для определения привкуса воды допускается приготовление анализируемого вещества в любых емкостях. 10 - 15 мл исследуемой воды набирается в рот и задерживается на 3 - 5 сек. (как, например, при дегустации вина), затем воду удаляют из полости рта. Качественно характеризуется вкус воды: соленый, кислый, горький, сладкий, или привкус: щелочной, терпкий, затхлый, металлический и т.д.
Интервал между определениями - не менее 2 - 3 мин.
6.4. Определение пороговых концентраций по запаху (привкусу) проводится при различных концентрациях вещества в воде. Исследования выполняются в две стадии.
6.4.1. На предварительной стадии применяется метод оценки запаха (привкуса) в баллах. С этой целью готовится исходный истинный раствор вещества, обладающий отчетливым запахом или привкусом. Ряд исследуемых образцов готовится путем последовательного разведения каждой пробы в 2 раза. Определение ведут в направлении от меньшей концентрации к наибольшей в ряду исследуемых проб, сопоставляя каждый образец с контрольной пробой. Опыты проводят в несколько серий с различными концентрациями вещества. Группа дегустаторов должна состоять не менее чем из пяти-семи человек.
6.4.2. Интенсивность запаха (или привкуса) оценивается по соответствующей шкале (табл. 6.1)
Таблица 6.1
ШКАЛА ИНТЕНСИВНОСТИ ЗАПАХА (ПРИВКУСА)
Характер проявления | Оценка интенсивности, баллов |
| Не ощущается | 0 |
| Не ощущается населением, но обнаруживается опытным дегустатором | 1 |
| Замечается населением, если обратить на это его внимание | 2 |
| Легко обнаруживается и вызывает неодобрительный отзыв о воде | 3 |
| Обращает на себя внимание и заставляет воздерживаться от питья | 4 |
| Настолько сильный, что делает воду непригодной для употребления | 5 |
Результаты обобщаются в виде сводной таблицы (табл. 6.2). На основании исходных данных рассчитывают среднегеометрические концентрации, соответствующие 1 и 2 баллам. За пороговую концентрацию рекомендуется принимать нижнюю доверительную границу средней величины, которая обеспечивает 95%-ную достоверность. Аналогичные расчеты применимы и для оценки влияния веществ на привкус воды.
Таблица 6.2
ОПРЕДЕЛЕНИЕ ИНТЕНСИВНОСТИ ЗАПАХА ВОДЫ С РАЗЛИЧНЫМ СОДЕРЖАНИЕМ В НЕЙ ПОЛИХЛОРПИНЕНА
Концентрация вещества, мг/л | Интенсивность запаха, баллов | |||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | M' | |
| 0,25 | 0 | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0,22 |
| 0,5 | 0 | 2 | 2 | 0 | 1 | 0 | 0 | 0 | 0 | 0,55 |
| 1 | 1 | 2 - 3 | 2 - 3 | 1 | 2 | 2 | 1 | 1 | 1 | 1,57 |
| 2 | 2 | 3 | 3 | 2 | 3 | 3 | 2 | 2 | 3 | 2,55 |
| 4 | 3 - 4 | 3 - 4 | 3 - 4 | 3 | 4 | 4 | 2 | 2 | 5 | 3,85 |
| 8 | 5 | 4 | 4 - 5 | 4 | 5 | 5 | 4 | 4 | 5 | 4,94 |
| М' - среднеарифметическое значение. | ||||||||||
Критерием гигиенического нормирования веществ является порог восприятия запаха (привкуса), соответствующий 1 баллу. Если в пределах растворимости вещества интенсивность запаха (привкуса) не превышает 1 - 2 баллов, исследования заканчиваются на первой стадии, а в результатах указывается: пороговая концентрация вещества по влиянию на запах (привкус) воды выше его концентрации на пределе растворимости.
6.5. Определение пороговых концентраций по влиянию на окраску, мутность воды проводится в столбе раствора высотой 10 и 20 см.
Используются 4 - 5 цилиндров Генера, которые устанавливаются на белой бумаге при равномерном освещении.
6.6. Пороговая концентрация по пенообразованию определяется с помощью градуированных цилиндров емкостью 1000 мл с притертыми пробками. В них наливается по 500 мл исследуемого раствора и контрольная вода. В течение 15 секунд производится 15 умеренно резких опрокидываний цилиндров - сначала контрольных, а затем опытного - и отмечается интенсивность пенообразования. За пороговую принимается концентрация, при которой отсутствует стабильная крупнопузырчатая пена, а высота мелкопузырчатой у стенок цилиндра не превышает 1 мм.
6.7. Определение пороговых концентраций по таким критериям, как посторонние включения или плавающие примеси, проводится в стакане объемом 500 мл, в который наливается 250 мл раствора, а в 4 других стакана - аналогичные растворы сравнения. Пороговым считается количество вещества, при котором не обнаруживается визуально ни одной видимой частицы в толще, на поверхности или на дне.
6.8. С целью получения более точных пороговых величин проводят вторую стадию исследований - "закрытый" опыт методом пятиугольника или, в крайнем случае, треугольника. "Закрытый" опыт используется для установления пороговых концентраций по запаху, привкусу, пленко- и пенообразованию, а также по влиянию на окраску воды.
Этот метод основан на принципе учета различной (дифференцированной) чувствительности человека при альтернативной оценке эффекта.
6.8.1. На основании первой стадии (п. 6.7) выбирается кратность последовательного разведения растворов <= 1,5, которая является оптимальной при определении ПК по запаху, привкусу, окраске, мутности и пенообразованию. При определении ПК по плавающим примесям, пленке допустима кратность 2,0. На основании первой стадии выбирают концентрации = 3 баллам.
6.8.2. Каждая опытная проба группируется с четырьмя - двумя контрольными пробами. Дегустаторам предлагается найти опытную пробу в каждой группе. Последовательность поиска опытной пробы - от меньшей концентрации к большей. Регистрируют результаты оценки проб, фиксируя номер колбы, которую дегустатор считает опытной. Подсчитывается процент дегустаторов, правильно указавших опытную пробу, из всего числа лиц, принимающих участие в опыте. Общее число наблюдений по определению каждой концентрации должно быть в пределах 30 - 50. Последовательно чередуются четыре - пять концентраций. Опыт можно считать законченным, если в ряду изученных концентраций процент правильных ответов варьировался в пределах от 20 - 30 до 60 - 80%. Иначе необходимо продолжить исследования.
Результаты опытов записываются в форме таблицы 6.3.
6.8.3. Анализ полученных данных выполняется или с помощью расчетов на компьютере, или графическим методом в двойном логарифмическом масштабе.
Проценты правильных положительных ответов для каждой испытанной концентрации веществ оцениваются так же, как результаты острых опытов в токсикологических исследованиях. Вычисляется величина среднеэффективной концентрации и ее ошибка (EC50 +/- m). Эту величину можно с достаточной надежностью рассматривать как порог ощущения.
При проведении исследований методом "закрытого" опыта следует учитывать вероятность случайности правильного ответа. Теоретически процент таких ответов при использовании метода пятиугольника может достигать 20, а для метода треугольника - 33.
Таблица 6.3
ВЛИЯНИЕ ТОЛУОЛА НА ЗАПАХ ВОДЫ
Концентрация толуола, мг/л | Количество наблюдений | Число положительных ответов | Положительные ответы, % |
| 0,1 | 80 | 60 | 75 |
| 0,075 | 40 | 19 | 47,5 |
| 0,05 | 48 | 15 | 31,2 |
| 0,0325 | 80 | 10 | 12,15 |
| контроль | 60 | 9 | 15 |
Для получения более точных результатов можно исключить эту ошибку, используя формулу Шнейдера-Орелли, предложенную для корректировки результатов острых опытов, но, как показала практика, приемлемую и для органолептических исследований:
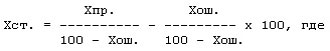
Хст. - стандартизованный процент правильных ответов;
Хпр. - экспериментально полученный процент правильных ответов;
Хош. - процент ошибочных ответов в данной группировке проб на одну контрольную пробу.
Величина EC50 по влиянию на запах, привкус, окраску, образование пленок, пены, мутности принимаются в качестве пороговых. Наименьшая из пороговых концентраций по тому или иному органолептическому показателю принимается за пороговую по органолептическому признаку вредности.
Абсолютно нерастворимые, несмачивающиеся вещества, относящиеся к 4-му классу токсичности (DL50 > 10000), не вызывающие изменений в кратковременных опытах в дозах > 500 мг/кг, могут нормироваться как взвешенные природные вещества на уровне 0,25 мг/л.
7. Экспериментальное установление пороговых концентраций веществ по влиянию на процессы самоочищения водных объектов
7.1. Санитарный режим водных объектов в зонах влияния выбросов сточных вод определяется интенсивностью процессов естественного самоочищения, в ходе которых происходит потребление кислорода, развитие и отмирание сапрофитной и патогенной микрофлоры, трансформация и минерализация органических соединений.
В общем виде процесс биохимического потребления кислорода происходит в 2 стадии: первая - окисление нестойких органических соединений - развивается довольно быстро и носит экспоненциальный характер; вторая - окисление стойких органических веществ - протекает в природных водах медленнее и, как правило, линейно. Интенсификация второй стадии потребления кислорода в скляночном опыте означает наступление активации окисления азотсодержащих веществ или адаптации микрофлоры к ассимиляции изучаемого вещества.
7.2. Целью экспериментального гигиенического исследования влияния вещества на процессы естественного самоочищения водных объектов является обобщенная оценка интенсивности и направленности взаимосвязанных фаз биохимического окисления естественных органических веществ (БПК, аммонификации, нитрификации, развития и отмирания микрофлоры), обоснование пороговых концентраций вещества по общесанитарному признаку вредности (ПКсан.).
7.3. Объем исследования дифференцируется в зависимости от задач и результатов комплексной оценки токсиколого - гигиенических свойств веществ.
7.3.1. Проводятся исследования БПК за 5 (7) суток в динамике: тотчас, через 1, 3 и 5 (7) суток и определяется ПКсан.
7.3.2. После установления ПКорг. и ПКхр. по санитарно - токсикологическому признаку вредности они сопоставляются с ПКсан. по БПК5(БПК7).
При ПКсан./ПКорг., ПКсан./ПКхр. >= 1 исследования процессов самоочищения могут считаться завершенными.
При ПКсан./ПКорг., ПКсан./ПКхр. < 1 необходимы уточняющие исследования с изучением влияния веществ на динамику содержания аммиака, нитритов и нитратов в воде модельных водоемов. При стимуляции БПК необходимо продолжить наблюдения на 7 - 10 - 15 - 20 суток.
7.3.3. Для уточнения характера влияния вещества на процессы естественного самоочищения в качестве дополнительных могут применяться методы исследования динамики развития и отмирания микрофлоры. Дополнительные исследования в модельных водоемах со стандартизованной водой позволят получить представление о воспроизводимости результатов.
Каждый показатель исследуется не менее чем в 3-х сериях опытов.
7.4. Выбор концентраций для опыта проводят по данным о растворимости и стабильности вещества, величине химического потребления кислорода в расчете на 1 мг вещества.
В первой ориентировочной серии допустимы различия между концентрациями вещества в 10 раз, в последующих 3-х сериях исследуют 3 - 4 концентрации, отличающиеся одна от другой в 3 - 4 раза. Контролем служит разводящая вода без вещества.
7.5. В связи с высокой вариабельностью процессов самоочищения как в скляночных опытах, так и в модельных водоемах необходимо соблюдение ряда требований к разводящей воде и правилам ее подготовки.
В качестве источника органических веществ естественного происхождения и активной сапрофитной микрофлоры используют хозяйственно-бытовую сточную воду, которая должна быть свободна от примесей ингредиентов промышленных сточных вод и взвешенных веществ. Длительное хранение (более 24 ч) хозяйственно - бытовой жидкости при температуре 20 град. C недопустимо. При проведении ориентировочных опытов готовая смесь этой жидкости с разводящей водой должна храниться в холодильнике при температуре 4 - 8 град. C. Перед началом эксперимента перманганатным методом определяют окисляемость водной смеси с хозяйственно - бытовой сточной жидкостью. Если величина окисляемости выше 15 мг О2/л, сточная вода разбавляется. В качестве разводящей воды используется дехлорированная водопроводная вода, свободная от веществ, оказывающих влияние на процессы БПК. Вода насыщается кислородом воздуха до концентрации 6,0 - 8,0 мг/л. Сосуды для этой воды нельзя использовать для других целей. Целесообразно, чтобы аэрированная вода имела температуру около 20 градусов.
После разбавления окисляемость смеси не должна превышать 8 - 9 мг О2/л.
7.6. Определение окисляемости, БПК, аммиака, нитритов, нитратов проводится общепринятыми методами [1].
В дополнительных исследованиях может использоваться стандартизованная разводящая вода.
Допускается изучение слаборастворимых веществ в смеси с ПАВ или в виде мелкодисперсной взвеси или эмульсии. Контролем при этом служит разводящая вода, содержащая соответствующее количество ПАВ.
7.7. Правильность постановки опыта проверяется по следующим критериям.
7.7.1. Величина БПК за первые сутки должна быть в пределах 0,7 - 1,2 мг/л, а к концу опыта - не менее 3 мг/л. Динамика процесса БПК выражается зависимостью, близкой к экспоненциальной, не наблюдается смена подъемов и снижений кривой. В двойном логарифмическом масштабе график зависимости представляет собой прямую.
7.7.2. Баланс уменьшения количества аммиачного азота, нарастания и убыли нитритного азота и нарастания азота нитратов (до 0,1 мг/л) должен сохраняться в каждый момент определения.
7.7.3. При длительных исследованиях динамики БПК дополнительная интенсификация процесса на 5 - 10 или 15 суток может быть отражением наступления второй стадии минерализации и сопровождаться накоплением нитратов в воде.
7.8. Результаты всех стадий исследований представляются в форме таблиц, а динамика БПК и динамика развития и отмирания микрофлоры - и в виде графиков.
7.9. При оценке экспериментальных данных выводы делаются на основании каждой серии в отдельности. В силу высокой вариабельности процессов в разных сериях, усреднение и статистическая обработка результатов не допускаются.
7.9.1. Высокая вариабельность процессов самоочищения не позволяет принимать во внимание отклонения от контроля < 15%. С гигиенических позиций процессы ингибирования самоочищения более опасны, чем стимуляция. Поэтому необходима дифференциация критериев вредности в зависимости от направленности нарушения первой стадии минерализации. При ее ингибировании за пороговую принимается концентрация вещества, вызывающая угнетение БПК на 15%, а при стимуляции - на 20%. При преимущественном влиянии вещества на вторую стадию минерализации критерием пороговой дозы является 15%-ное отклонение от контроля.
7.9.2. Если при наименьшей из действующих концентраций БПК отличается от контроля больше или меньше чем на 15% (или 20%), пороговую концентрацию можно рассчитать на основании линейной полулогарифмической зависимости "концентрация-эффект" графическим или статистическим методом и, таким образом, получить более точную величину ПКсан.
7.9.3. Для уточнения величин пороговых концентраций при стимуляции БПК можно определить, сколько в процессе биохимического окисления приходится кислорода на 1 мг изучаемого вещества:
![]()
А - количество кислорода на 1 мг изучаемого вещества;
БПКх - БПК в опыте, последний срок наблюдения;
БПКк - БПК в контроле в последний срок наблюдения;
С - концентрация изучаемого вещества (мг/л).
Правилами охраны поверхностных вод от загрязнения предусмотрено, что в воде водных объектов должен содержаться растворенный кислород в количестве не менее 4 - 6 мг/л. Поэтому применительно к натурным условиям при благоприятном санитарном режиме водного объекта без заметного ущерба для санитарного состояния водного объекта может быть использовано не более 1 - 2 мг/л кислорода. Тогда пороговая концентрация вещества ориентировочно может быть рассчитана по формуле:
![]()
А - количество кислорода на 1 мг изучаемого вещества.
Поскольку эта формула не в полной мере отражает реальное влияние сточных вод на санитарный режим водных объектов, предложена более точная формула:
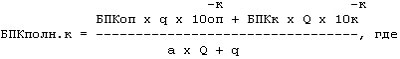
Q - расход воды водного объекта, куб. м/с;
q - расход сточных вод, в составе которых сбрасывается нормируемое соединение, куб. м/с;
a - коэффициент смешения сточных вод с водой водного объекта.
7.9.4. Для расчетного прогноза условий спуска сточных вод, содержащих вещества, нормируемые по общесанитарному признаку вредности и стимулирующие потребление кислорода, важно определение константы скорости потребления кислорода:
![]()
БПКt и ВПК2t - биохимическое потребление кислорода для 2-х сроков инкубации, кратных между собой;
K - искомая константа скорости;
t - время, сут.
8. Установление параметров токсичности веществ в острых опытах на животных
Установление смертельных эффектов позволяет получить необходимую информацию для решения ряда задач:
- определение параметров токсичности и опасности вещества при однократном (кратковременном) воздействии, а также получение первичной информации о характере и направленности действия;
- сравнительная оценка токсичности нескольких веществ, близких по физико-химическим свойствам или по условиям применения;
- установление видовой, половой и возрастной чувствительности лабораторных животных к действию вредного вещества;
- получение предварительной информации о способности вещества к материальной и/или функциональной кумуляции;
- сравнительная оценка токсичности исходного вещества и продуктов его трансформации в водной среде;
- получение информации, необходимой для выбора доз, исследуемых в подостром и хроническом экспериментах;
- определение правомерности применения корреляционных уравнений количественной зависимости "структура-активность" для прогноза параметров токсикометрии изучаемого вещества;
- установление зависимости "доза-ответ" и расчет средней смертельной дозы DL50.
Доза средняя смертельная - это количество яда, вызывающее гибель 50% группы подопытных животных за определенный период последующего наблюдения. Поскольку DL50 является статистической величиной, определяются также средняя ошибка и доверительные интервалы.
Другие показатели, например, DL100 (наименьшая доза, вызывающая гибель всех взятых в опыт животных) и DL0 (максимальная переносимая доза) определяются эмпирически, а не статистически, и поэтому могут использоваться как дополнительные ориентировочные величины.
8.1. Вещество изучается при следующих путях поступления в организм: при введении в желудок, нанесении на кожу.
Токсичность при внутрижелудочном введении определяется в опытах на животных (белых мышах массой 18 - 24 г, белых крысах массой 180 - 240 г, половозрелых морских свинках массой 350 - 500 г, кроликах массой 1,5 - 3,0 кг).
8.2. Выбор доз для исследования осуществляется:
- по аналогии с данными о токсичности близких по структуре веществ;
- расчетным путем по математическим моделям;
- в ориентировочном эксперименте.
В ориентировочном эксперименте устанавливается зона смертельного действия - отношение абсолютной смертельной дозы к минимальной смертельной или максимальной переносимой. Затем выбирается ряд доз, например, в соответствии с рядами Фульда:
1,0; 1,3; 1,8; 2,4; 3,2; 4,2; 5,6; 7,5; 10,0; 13,0
1,0; 1,3; 1,7; 2,1; 2,8; 3,6; 4,6; 6,0; 7,7; 10,0; 13,0
1,0; 1,3; 1,6; 2,0; 2,5; 3,2; 4,0; 5,0; 6,3; 8,0; 10,0.
Ориентировочная DL50 может быть установлена методом одной - двух точек или путем испытания ряда последовательных доз на 1 - 2 подопытных животных.
8.3. Количество животных в развернутом опыте должно быть достаточным для статистических расчетов. Каждая доза испытывается не менее чем на 10 белых мышах, белых крысах, на 6 морских свинках, кроликах и других животных.
8.3.1. Вещество в каждой из выбранных доз (а для соединений 3 и 4 классов стабильности и ранее не нормированные продукты трансформации) вводится с помощью зонда однократно в водном растворе, при малой растворимости в воде - в растительном масле. Может быть применен "универсальный" растворитель - диметилсульфоксид. Труднорастворимые, вязкие, смоло-, порошкообразные вещества можно вводить в виде взвесей или эмульсии в яичном желтке, 1 - 2%-ном растворе крахмала, с добавлением нетоксичных поверхностно-активных веществ. В отдельных случаях допустимо использование других растворителей: этанола, глицерина, полипропиленгликоля и т.п. Обязательное условие - введение контрольным животным используемого растворителя в эквивалентных количествах.
8.3.2. Для создания необходимых доз предпочтительнее вводить разные объемы раствора вещества одной концентрации. Вместе с тем, объем водных растворов не должен превышать 1 - 1,5%, а масляных - 0,5 - 1% от веса тела. Вещество вводится через 2 - 3 часа после кормления. Через 3 - 4 часа после введения вещества допускается очередное кормление животных.
8.3.3. Максимальная вводимая доза в желудок - 10 г/кг. При испытании малотоксичных веществ, не приводящих к гибели при однократном введении, допустимо вводить вещество несколько раз в максимально возможной концентрации в объеме <= 5%, а масляные растворы до 2% от веса тела с интервалом между введениями не менее 1,5 часов. Следует учитывать и предотвращать возможное местное раздражающее действие веществ, испытывать нейтрализованные растворы при условии, что это не приведет к разрушению и трансформации структурной части молекулы, определяющей токсичность вещества.
8.4. Наблюдение за животными продолжается в течение 14 дней после введения вещества. Фиксируется время гибели каждого животного (в первые сутки - в часах), общее количество погибших. Результаты заносятся в таблицу (табл. 8.1). Подробно описывается клиническая картина отравления, желательно - морфологические изменения внутренних органов и тканей. Делаются предварительные выводы о характере токсического действия вещества.
Таблица 8.1
ДИНАМИКА ГИБЕЛИ ЖИВОТНЫХ ПОСЛЕ ОДНОКРАТНОГО ВВЕДЕНИЯ ВЕЩЕСТВА В РАЗЛИЧНЫХ ДОЗАХ
Дозы, мг/кг | Число животных в группе | Число погибших животных по срокам наблюдения в часах (сутках) | Общее число погибших животных | % гибели | |||
8.5. Токсичность при накожном нанесении изучается согласно [1].
8.6. Расчет DL50 и доверительного интервала может проводиться любым из статистических методов, т.к. различия между величинами по результатам расчета значительно меньше, чем по экспериментальным данным, полученным в разных условиях. Более точным считается метод Литчфилда-Уилкоксона.
8.7. Для веществ из малоизученных классов необходимо определять сравнительную половую и видовую чувствительность на 4-х видах лабораторных животных, для остальных веществ - на 2-х видах. Определение острой токсичности на морских свинках, кроликах, кошках (в особых случаях) допустимо методом 1 - 2 точек. Метод дает возможность рассчитать ошибку и доверительные интервалы величин DL50.
8.8. Для получения сопоставимых результатов целесообразно стандартизовать условия эксперимента по виду, полу, возрасту, условиям содержания животных. С другой стороны, не следует чрезмерно уточнять их путем увеличения числа животных, уменьшения шага между дозами, усложнения методов расчета.
8.9. При оценке результатов острых опытов могут использоваться классификации токсичности, представленные в таблице 8.2.
Кроме того, необходим анализ кривых "доза-ответ", которые могут соответствовать не только функции нормального распределения, но и гиперболе, параболе, экспоненциальной кривой. Угол наклона кривых к оси абсцисс может дать информацию об общности или, наоборот, резких различиях в механизме токсического действия ряда веществ или на различные виды животных.
Пологая кривая чаще всего свидетельствует о плохом всасывании, быстром выведении или трансформации, или о наличии резких различий в индивидуальной чувствительности. Выраженная крутизна наклона свидетельствует об активном всасывании, быстром развитии токсического эффекта, а также о незначительных различиях в индивидуальной чувствительности.
Таблица 8.2
КЛАССИФИКАЦИЯ ТОКСИЧНОСТИ ПО СМЕРТЕЛЬНЫМ ЭФФЕКТАМ
Показатели токсикометрии, мг/кг | Классы токсичности | |||
| 1 | 2 | 3 | 4 | |
| 1. DL50 в/ж | < 100 | 100 - 1000 | 1001 - 10000 | > 10000 |
| 2. DL50 при нанесении на кожу | < 100 | 100 - 500 | 501 - 2500 | > 2500 |
8.10. Дополнительно по данным острого опыта рассчитываются параметры, дающие первое представление о способности веществ к кумуляции: среднее время гибели (TL50) и индекс кумуляции [1].
8.10.1. Для определения TL50 сопоставляется рабочая таблица, аналогичная таблице учета результатов острого опыта, сроки гибели животных выражаются в часах. По таблице подсчитывается суммарное время гибели животных от каждой из испытанных доз (Sumt), из которых находят среднее время гибели одного животного (tn) по формуле: tn = Sumt/n, где n - общее количество животных, погибших от данной дозы. TL50 рассчитывают теми же статистическими методами, что и среднесмертельную дозу или строят прямоугольную систему координат (в логарифмическом масштабе), откладывая по оси абсцисс время гибели животных (в часах), а по оси ординат - изученные в опыте дозы вещества (в мг/кг). На график наносят точки, соответствующие ранее найденным значениям tn, и через них проводят прямую, по которой находят TL50 - время гибели животных от дозы, равной DL50.
Таблица 8.3
КЛАССИФИКАЦИЯ ВЕЩЕСТВ ПО СПОСОБНОСТИ К КУМУЛЯЦИИ В ОСТРЫХ ОПЫТАХ
Степень кумуляции | Показатели кумуляции | Прогноз МНД по индексу кумуляции | |
| I | TL50, ч | ||
| 1. Сверхкумуляция | > 0,5 | > 48 | 1/250000 DL50 |
| 2. Сильная | 0,1 - 0,5 | > 24 - 48 | 1/50000 DL50 |
| 3. Средняя | < 0,1 | 12 - 24 | 1/10000 DL50 |
| 4. Слабая | 0 | < 12 | 1/2000 DL50 |
По таблице 8.3 определяют, к какому классу по способности к кумуляции относится вещество. Если TL50 находится в пределах 12 - 48 часов, допустимо применять расчетные уравнения для прогноза ПДхр. и МНД в соответствии с [4].
8.10.2. Для определения индекса кумуляции рассчитываются величины DL50 за 1 сутки (Д1) и по результатам гибели животных в течение всех 14 дней опыта (Д2). Затем определяют I:
I = I - Д2/Д1.
Классификация способности веществ к кумуляции и ориентировочные величины МНД приведены в таблице 8.3.
9. Порог вредного действия при однократном поступлении вещества в организм
Цели исследований:
- определить верхний предел доз для подострого эксперимента и оптимальное время наблюдения после введения вещества;
- получить характеристику кумулятивных свойств;
- при необходимости - изучить токсикокинетику и процесс детоксикации вещества;
- рассчитать зону острого действия.
9.1. Порог однократного действия определяется на белых крысах по интегральным и специфическим показателям с обязательным определением изменений в динамике в течение суток (или нескольких суток - в зависимости от TL50). Время первого определения устанавливается исходя из клинической картины отравления в остром опыте, но не позднее двух часов, затем, например, через 4 - 6 - 12 - 24 часа после затравки, а также через 2 - 4 и 8 дней после нее. Возможны и другие сроки наблюдения с учетом токсикодинамики и/или токсикокинетики. Порог однократного действия может быть установлен эмпирически или рассчитан как вероятностная величина (Limac) или дополнен результатами токсикокинетических исследований.
9.2. Для специальных научных целей можно определить кинетику накопления и выведения вещества и/или его метаболитов в организме.
9.3. На основании исследования зависимости "время - эффект" можно определить время полуубыли (тау) регистрируемого эффекта по формуле:
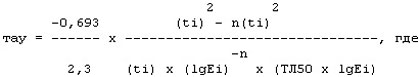
Еi - среднее значение степени эффекта (в % к параллельному контролю) в моменты времени ti (i - 1; 2; ...; n);
0,693 - натуральный логарифм из 2;
2,3 - коэффициент перехода от натуральных логарифмов к десятичным.
Степень кумуляции определяют по величине тау: при тау < 12, 12 - 24, 24 - 48 и > 48 часов кумулятивные свойства оценивают как слабые, средние, сильные и очень выраженные соответственно.
9.4. Пример определения пороговой дозы однократного действия в опыте с ацетонциангидрином (АЦГ).
При выборе доз и сроков наблюдения исходили из результатов острого опыта:
ЛД50 = 18,5 (16,9:20,3) мг/кг, TL50 = 85 мин. Первые признаки отравления появлялись через 10 - 15 мин. после введения ацетонциангидрина. Эти данные свидетельствуют о быстром развитии токсического процесса и слабо выраженной кумуляции.
Поэтому выбран минимальный интервал между дозами. Вещество вводилось однократно белым крысам в дозах, составляющих 1/5, 1/10, 1/15, 1/20 и 1/45 DL50. Отбор исследуемого материала /кровь, печень/ производили через 15, 30 мин., 1, 2, 4 и 6 часов после введения АЦГ. Контролем служили интактные животные. Поскольку механизм токсического действия цианидов хорошо известен, исследовались только специфические показатели: содержание оксигемоглобина и роданидов в крови, активность цитохромоксидазы печени. Установлено, что максимальный токсический эффект (пик содержания оксигемоглобина и снижение активности цитохромоксидазы) для доз 1/5, 1/10, 1/15 DL50 наблюдается через 30 мин. после введения вещества, а с уменьшением дозы (1/20, 1/45 DL50) срок достижения наибольших изменений увеличивается до 1 часа. Получены кривые зависимости "время - эффект" для разных доз.
По наиболее чувствительному показателю (изменению активности цитохромоксидазы) установлен порог однократного действия Limac, равный 1/45 DL50 (0,41 мг/кг). Зона острого действия DL50/Limac = 45. Это доказывает, что способность АЦГ к кумуляции слабо выражена.
Исходя из полученных данных для подострого эксперимента были выбраны дозы < Limac, т.е. 0,4; 0,08; 0,015 мг/кг с пятикратным шагом между ними.