АРОМАТИЧЕСКИЕ ПОЛИСУЛЬФОНЫ: получение и применение
Ароматические полисульфоны являются инженерными (конструкционными) термопластами, имеющими в основной цепи сульфоновые группы –SO2–.

Три представителя этого класса полимеров имеют промышленное значение: полисульфон (ПС), полиэфирсульфон (ПЭС), полиарилсульфон (ПФС). Кроме сульфоновых групп в основной цепи этих полимеров имеются простые эфирные связи, алифатические и ароматические фрагменты в различном сочетании.
Сульфоновые полимеры являются аморфными термопластами с высокими эксплуатационными характеристиками. Гидролитическая устойчивость полисульфонов позволяет применять эти полимеры в изделиях контактирующих с водой и водяным паром. Химическая стабильность дает полисульфонам возможность работать в кислых и щелочных средах. Благодаря высоким температурам стеклования и термостабильности максимальная температура длительной эксплуатации полимеров этого ряда составляет: ПС – 150°С, ПЭС – 180°С, ПФС – 190°С.
Отличительной особенностью всего ряда ароматических полисульфонов является их высокая огнестойкость, низкая плотность дымовыделения, химическая стойкость во многих агрессивных средах и растворителях. Наиболее значимыми областями применения ароматических полисульфонов являются: электроника, электротехника, авиакосмическая промышленность, транспортное машиностроение, медицинское оборудование, бытовая техника, строительство.
Синтез ароматических полисульфонов осуществляется методом ароматической нуклеофильной поликонденсации в апротонных растворителях. В качестве растворителей, как правило, используют диметилсульфоксид, диметилацетамид, N-метилпирролидон, диметилсульфон, дифенилсульфон. Для получения щелочных солей бисфенолов применяют гидроокись натрия или углекислый калий. Поликонденсацию ведут при температуре 160 – 3200С в зависимости от применяемого растворителя и реакционной способности мономеров. Полисульфон получают взаимодействием щелочной соли бисфенола-А с сульфонсодержащим мономером, 4,4'-дихлор-дифенилсульфоном:
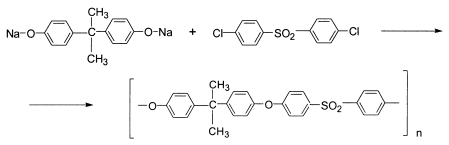
Полиэфирсульфон получают реакцией 4,4'-диоксидифенил-сульфона в виде щелочной соли с 4,4'-дихлордифенилсульфоном:
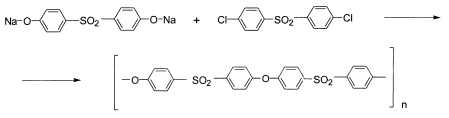
Полифенилсульфон получают реакцией 4,4'-диоксидифенила и 4,4'-дихлордифенилсульфона:
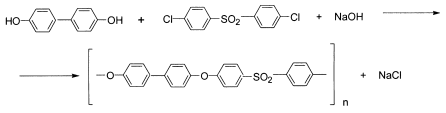
В качестве исходных мономеров для получения ароматических полисульфонов кроме дифенилолпропана, 4,41-диоксидифенилсульфона и 4,41-диоксидифенила наиболее известны такие бисфенолы как фенолфталеин, гидрохинон, 4,41-(диоксифенилсульфонил)-бифенил. В качестве дигалогенарилсульфонов используют: 4,41-дихлордифенилсульфон, тетрахлордифенилсульфон, 4,41-(дихлорфенилсульфонил)-бифенил.
Исследования в области ароматической нуклеофильной поликонденсации с целью разработки оптимальных методов синтеза ароматических полисульфонов проводились группами химиков ряда таких ведущих стран, как США, Германия, Великобритания.
В России ведущей организацией по созданию технологии ароматических полисульфонов и дигалогенарилсульфонов (мономеров) является Научно-исследовательский институт пластических масс им. Г.С.Петрова, в котором в конце 1976 г. была создана лаборатория химии и технологии полисульфонов. Главной задачей этой лаборатории являлась разработка технологии получения полисульфона (ПС) на основе дифенилолпропана и 4,41-дихлордифенилсульфона, а также проведение исследований в области синтеза ароматических полисульфонов, превосходящих по некоторым свойствам полисульфон на основе дифенилолпропана.
К исследованиям в этой области были подключены сотрудники физико-химического, аналитического, физико-механического и инженерного отделов. К работам по синтезу мономеров привлекали также Ярославский политехнический институт, Киевский филиал ГосНИИХлорпроекта, Всесоюзный научно-исследовательский институт полупродуктов и мономеров (г. Тула) и некоторые другие институты. За период с 1977 г. по 1989 г. был выполнен значительный объем исследований как в области синтеза полисульфонов, так и синтеза мономеров. Основные результаты выполненных в этот период работ опубликованы в ряде научных журналов [1–14].
В области ароматической нуклеофильной поликонденсации была изучена кинетика реакции динатриевой соли дифенилолпропана с 4,41-дихлордифенилсульфоном в диметилсульфоксиде. Это исследование показало, что реакция поликонденсации имеет сложный характер, определяющийся как значительной разницей в скорости взаимодействия первой и второй гидроксильных групп дифенилолпропана и первым и вторым хлором 4,41-дихлордифенилсульфона, так и изменением реологических свойств реакционной среды по мере нарастания молекулярной массы полисульфона.
Изучение гидролиза 4,41-дихлордифенилсульфона гидроокисью натрия и углекислым калием в диметилсульфоксиде, диметилацетамиде и N-метилпирролидоне выявило преимущества использования более слабого щелочного агента при синтезе полисульфонов. Различными физико-химическими методами был исследован состав и строение полимерной цепи полисульфона. При исследовании строения полимерной цепи полисульфона установлено, что в присутствии гидроокиси натрия в безводной среде происходит частичное алкилирование бензольного кольца демсилом натрия, образующимся при взаимодействии диметилсульфоксида с гидроокисью натрия.
Впервые показано наличие в полисульфоне циклических олигомеров с различным размером циклов. Методом масс-спектрометрии идентифицированы макроциклы содержащие от одного до шести элементарных полимерных звеньев. Очевидно, что реакция циклизации при синтезе полисульфонов является общей для полимеров этого ряда, так как даже кардовый полисульфон на основе фенолфталеина и дифенилолпропан содержит макроциклы. Установлено, что при синтезе полисульфона на основе дифенилолпропана и 4,41-дихлордифенилсульфона преимущественно образуется макроцикл, имеющий следующее строение:
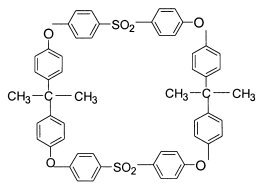
Определен характер влияния макроциклов на свойства полисульфона и показаны условия, способствующие их образованию при синтезе. При разработке технологического процесса получения полисульфона определены основные термодинамические, теплофизические и реологические характеристики исходных мономеров, промежуточных реакционных сред на всех стадиях процесса и конечных продуктов.
Разработанный технологический процесс [15–28] производства полисульфона был реализован на опытно-наработочной установке НИИПМ, где были не только уточнены параметры отдельных стадий процесса, но и производился серийный выпуск порошкообразного полисульфона для пленочных клеев.
В 1984 г. было пущено промышленное производство полисульфона мощностью 200 т/год на Шевченковском заводе пластмасс (Казахстан) и производство мономера 4,41-дихлордифенилсульфона мощностью 300т/год на ПО «Капролактам» (г. Дзержинск, Нижегородской обл.). В 90-х годах коллектив лаборатории понес значительные материальные и моральные потери, производства полисульфона и 4,41-дихлордифенилсульфона были закрыты. Тем не менее, лаборатория продолжала работать.
В этот период были продолжены исследования по химии и кинетике поликонденсации в диметилацетамиде, реологии растворов полисульфона и полиэфирсульфона в диметилацетамиде, хлорбензоле и N-метилпирролидоне. В результате этих работ была создана новая универсальная технология получения полисульфонов [29], позволяющая снизить энергоемкость процесса, уменьшить количество отходов и повысить качество готовых продуктов. Эта технология дает возможность получать по единой технологической схеме и на одном технологическом оборудовании целый ряд полисульфонов, в том числе полисульфон, полиэфирсульфон, полиарилсульфон и сополисульфоны различного состава.
В 2000–01г.г. проведена реконструкция опытно-наработочного производства и начат выпуск порошкообразного полисульфона клеевого назначения марок ПСК-1 и ПСК-2 по новой технологии. В настоящее время основным направлением работ лаборатории полисульфонов является исследование возможностей химической модификации полимеров сульфонового ряда. Путем введения в основную полимерную цепь новых фрагментов получены сополимеры содержащие кардовые группы (сополимеры серии ПСФФ) и полисульфидсульфоны (серия ПСФС). Процесс получения кардовых полисульфонов может быть представлен следующей схемой:
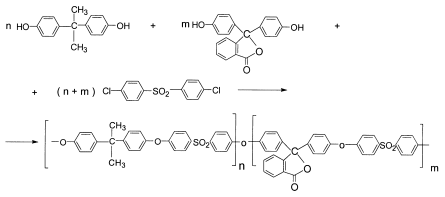
Синтезирован ряд кардовых сополисульфонов с содержанием кардовых звеньев до 100%. С увеличением содержания кардовых звеньев в цепи полисульфона повышается температура стеклования полимера до 256°С, при этом полимер сохраняет текучесть вплоть до 380°С.
Синтез полифениленсульфонсульфидов осуществляли в диметилацетамиде в присутствии углекислого калия в две стадии. На первой стадии 4,41-дихлордифенилсульфон реагирует с сульфидом натрия, на второй – с дифенилолпропаном по схеме:
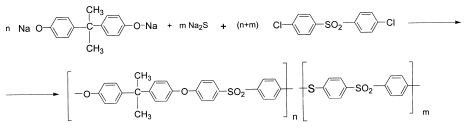
Была синтезирована серия полифениленсульфидсульфонов с содержанием сульфидных фрагментов до 50%. Температура стеклования сульфонсульфидов при увеличении содержания сульфидных фрагментов изменяется незначительно в интервале от 185 до 197°С.
Проводятся исследования в области синтеза сульфированных, эпоксидированных и гидрофилизированных полисульфонов. Положительные результаты этих работ дают возможность расширить области применения полисульфонов в различного рода мембранных процессах, а также повысить теплостойкость этих полимеров, снизить их горючесть, тепло- и дымовыделение, а в клеевых марках увеличить адгезию к стеклу и металлам.
Некоторые из перечисленных научных разработок в настоящее время находятся на стадии выпуска опытных партий и их испытания в конкретных изделиях. В результате комплексных исследований в области химии и технологии ароматических полисульфонов, которые проводятся в институте более двадцати лет, а также на основе опыта приобретенного при создании и эксплуатации опытно-наработочной установки и промышленного производства полисульфонов, были разработаны три варианта технологии, блок-схемы которых приведены в таблице:
Таблица 1.
Сравнительные блок-схемы производства полисульфона.
| Вариант-1 | Вариант-2 | Вариант-3 |
| Приготовление растворов мономеров | отсутствует | отсутствует |
| Азеотропная сушка фенолята | отсутствует | отсутствует |
| Поликонденсация | Поликонденсация | Поликонденсация |
| Перерастворение в хлорбензоле | Разбавление | Разбавление |
| Отстаивание и разделение растворов | Фильтрация от соли | Фильтрация от соли |
| Водные промывки | Высаждение в воду | Отсутствует |
| Обработка сорбентом и фильтрация | Промывка порошка водой | Отсутствует |
| Концентрирование на роторно-пленочном испарителе | Сушка порошка в вакуум-гребковой сушилке | Концентрирование на роторно-пленочном испарителе |
| Концентрирование в фильмтрудере I и II ступени | Концентрирование в фильмтрудере I и II ступени | |
| Грануляция (экструдер) или III-ступень фильмтрудера | Грануляция (экструдер) или III-ступень фильмтрудера | Грануляция (экструдер) или III-ступень фильмтрудера |
| Регенерация смеси ДМСО-вода и хлорбензола | Регенерация смеси ДМАА-вода | Отсутствует |
Реализованная на первом этапе технология синтеза полисульфона в диметилсульфоксиде (вариант I) являлась многостадийной и сложной в аппаратурном оформлении. Кроме того, неудовлетворительная растворимость полимера в диметилсульфоксиде делала невозможной фильтрацию его от образовавшейся в процессе синтеза соли, поэтому требовалось перерастворение реакционной массы в хлорбензоле, в растворе которого проводилась отмывка от диметилсульфоксида и соли. Выделение полисульфона проводили методом ступенчатого концентрирования до расплава с последующей грануляцией. Процесс был реализован на опытно-промышленной установке мощностью 200 т/год, работавшей с 1984 г. по 1993 г.
На опытно-наработочной установке НИИПМ производился выпуск порошкообразного полисульфона по варианту 1, но выделение полимера в виде порошка производили из реакционной массы. Разработка технических решений по синтезу полисульфона в среде амидных растворителей позволила значительно упростить технологическую схему и иметь возможность выделять полимер как в виде порошка, так и гранулята (варианты II и III). При этом исключалась необходимость применения стадий перерастворения в хлорбензоле и его регенерации. Одновременно с этим упростилось аппаратурное оформление стадии отмывки полимера от растворителя при его выделении в виде порошка.
Синтеза полисульфонов в амидных растворителях по варианту II реализован на опытно-наработочной установке мощностью до 5 т/год после ее реконструкции. Оценивая все перечисленные варианты с точки зрения их экономичности, следует признать наиболее эффективным промышленную реализацию по варианту III. Учитывая, что аппаратурное оформление каждой из стадий этого варианта проверено на пилотных установках при реализации вариантов I и II, эта технология была заложена в проект производства мощностью 400т/год для ОАО «Тверьхимволокно».
Достоинством разработанных технологических процессов является возможность получать полисульфоны как в виде гранул, так и в виде порошка, что расширяет области применения этих полимеров, в частности для получения пленочных клеевых композиций.
Производство и потребление полисульфонов в США и в Западной Европе.
Нижеприведенные таблицы характеризуют производственные мощности фирмы Амоко, единственного производителя сульфоновых полимеров в США [30].
Таблица 2,
Производство сульфоновых полимеров в США.
| Компания и место расположения | Мощность тыс.т. на 1998 г. | Продукты | Наименование марок |
| Амоко Корп. Мариэтта, Огайо | 13,8 с 2001г. 20,6 4,0-4,7 | Полисульфон Полиарилсульфон Полиэфирсульфон | Udel Radel A и Radel R |
| всего | 24,5–25,3 |
С третьего квартала 1998 года фирма начала работы по увеличению мощности полисульфонов с 16 тыс. т/год до 24 тыс. т/год. Сравнительный рост потребления сульфоновых полимеров в США в период 1985 по 1998 гг. приведен в таблице 3.
Таблица 3.
Потребление сульфоновых полимеров в США. (тыс.т.)
| Годы | Электроника, электротехника | Пищевая | Транспорт | Медицина | Космос, авиация | Всего |
| 1985 | 1,1 | 0,6 | 0,4 | 0,3 | 0,6 | 3,0 |
| 1988 | 2,0 | 0,9 | 0,7 | 0,6 | 0,9 | 5,1 |
| 1991 | 2,1 | 1,8 | 1,15 | 0,9 | 0,9 | 6,85 |
| 1995 | 3,6 | 2,6 | 1,8 | 1,6 | 1,0 | 10,6 |
| 1997 | 4,5 | 3,4 | 2,5 | 2,15 | 1,2 | 13,75 |
| 1998 | 4,3 | 3,6 | 2,6 | 2,3 | 1,3 | 14,1 |
| 1999 | 5,0 | 3,95 | 2,96 | 2,6 | 1,46 | 16 |
| 2000 | 5,6 | 4,55 | 3,5 | 3,0 | 1,75 | 18,4 |
| 2001 | 6,0 | 5,0 | 3,6 | 3,4 | 1,8 | 19,8 |
Следующая таблица представляет динамику цен за период 1985–1998 гг. на наиболее массовые полимеры сульфонового ряда.
Таблица 4.
Цены на рынке США, $/кг.
| Полисульфон | Полиэфирсульфон | |||||
| Годы | Udel P-170 | Udel GF-20 | Mindel S-1000 | Ultrason E 2010 | Ultrason E 2010 G4 | Radel A-200 |
| 1985 | 8,5 | 7,6 | - | - | - | - |
| 1988 | 8,6 | 7,8 | - | - | - | - |
| 1992 | 8,9 | 8,5 | 6,8 | 11,2 | 9,9 | - |
| 1995 | 9,6 | 9,1 | 7,4 | 13,2 | 12,7 | - |
| 1998 | 10,5 | 9,8 | 8,5 | 14,3 | 13,8 | 14,2 |
| 2002 | 12 | 11,5 | 10,7 | 16,5 | 15,6 | 20,0 |
В 1997 году США экспорт сульфоновых полимеров составил 5,2 тыс. тонн из этого количества 31% (1,6 тыс.т) для Бельгии, 26% (1,4 тыс.т) для Пуэрто-Рико, 19% (1,1 тыс.т) для Японии.
Западная Европа.
В Западной Европе единственным производителем сульфоновых полимеров является фирма БАСФ, которая выпускает полисульфон и полиэфирсульфон под марками Ultrasou-S и Ultrasou E.
Общие объемы производства сульфоновых полимеров в Западной Европе представлены в таблице 5.
Таблица 5.
Производство сульфоновых полимеров в Западной Европе, (тыс.т.).
| 1988 | 2,0 |
| 1991 | 1,15 |
| 1995 | 1,4 |
| 1997 | 1,6 |
| 2001 | 2,4 |
Объемы потребления сульфоновых полимеров в Западной Европе представлены в таблице 6.
Таблица 6.
Потребление сульфоновых полимеров в Западной Европе, (т).
| Годы | Полисульфон | Полиэфирсульфон | Всего |
| 1980 | 600 | 200 | 800 |
| 1985 | 870 | 500 | 1370 |
| 1988 | 1,065 | 1000 | 2065 |
| 1991 | 1400 | 1100 | 2500 |
| 1995 | 1960 | 1540 | 3500 |
| 1997 | 2580 | 1720 | 4300 |
| 2000 | 3500 | 2700 | 6200 |
| 2001 | 4133 | 2755 | 6888 |
| 2006 | 6075 | 4050 | 10125 |
При этом разбивка по областям применения сохранялась практически стабильной в течение всего периода и составляла при общем росте потребления следующие величины:
Электроника/электротехника ― 50%
Транспорт ― 23%
Медицина ― 12%
Космос-авиация ― 7%
Другие ― 8%
Цены сульфоновых полимеров на Европейском рынке приведены в таблице 7.
Таблица 7.
Цены в Западной Европе, $/кг.
| Полимер | 1995 | 1998 | 2001 | |
| Полисульфон | 13,95 | 15,5 | 13,85 | 14,7 |
| Полиэфирсульфон | 21,2 | 20,3 | 17,8 | 19,5 |
прирост объемов потребления отмечается в таких областях промышленности, как электроника, электротехника, пищевая, медицинская и строительная.
Литература
1. Лущейкин Г.А. и др., Пластич.массы,1989, 2, с.37.
2. Любарова Л.Г. и др., Пластич.массы,1988,10, с.12.
3. Куличихин С.Г. и др., Пластич.массы,1988, 6, с.41.
4. Плешкова А.П. и др., Высокомолек.соед.,1986,т.28, 9,с.2005.
5. Наркон А.Л.и др., Высокомолек.соед.,1986,т.28, 3,с.505.
6. Ключников В.Н. и др., Высокомолек.соед.,А ,т.26, 8,с.1718.
7. Наркон А.Л.и др., Высокомолек.соед.,А, 1984, 8,с.1712.
8. Булай А.Х.и др., Высокомолек.соед.А, 1982, 5,с.1078.
9. Слоним И.Я. и др., Высокомолек.соед., Б, 1980, т.22, с.9, с.644.
10. A.Kh.Bulai et al., Polymer,1987,Vol 28, July , p 1349.
11. Наркон А.Л.и др., Высокомолек.соед.,Б, 1982, т.26, 8, с.616
12. Малкин А.Я. и др., Высокомолек.соед.,Б, 1982 , т.24, 7, с.710.
13. Рейтбурд Л.И. и др., Пластич.массы., 1980, 9, с.41.
14. Семенкова А.Э. и др., Пластич.массы, 1984, 4, с 26.
15. Болотина Л.М. и др., А.с.№ 273 818, 1987
16. Болотина Л.М. и др., А.с.№ 639 874, 1977.
17. Рейтбурд Л.И. и др., А.с.№ 773 050,1978.
18. Григорьянц И.К.и др., А.с.№ 803 683, 1979.
19. Богачев Г.В. и др., А.с.№ 826 724, 1981.
20. Болотина Л.М.и др., А.с. № 924 771, 1982.
21. Москвичев Ю.А. и др., А.с.№ 948 099, 1982.
22. Болотина Л.М. и др., А.с.,№ 952 923, 1982.
23. Болотина Л.М.и др., А.с.,№ 976 680, 1982.
24. Лебедев Н.А. и др., А.с.,№ 1 023 782, 1983.
25. Шлепнева Н.Д. и др., А.с.,№ 1 023 783, 1983.
26. Карпенко Л.А. и др., А.с.,№ 1 051 902, 1983.
27. Болотина Л.М. и др., А.с., № 1 329 157, 1984.
28. Уродовская Н.И. и др., А.с., № 1 490 918, 1987.
29. Болотина Л.М., Чеботарев В.П., патент РФ № 2 063 404, 1994
Л.М. Болотина, В.П. Чеботарев
Научно-исследовательский институт пластических масс им. Г.С. Петрова
Пластические массы