КАПРОЛАКТАМ: свойства и области использования
Капролактам (гексагидро-2-азепинон, лактам e-аминокапроновой к-ты, 2-оксогексаметиленимин).
Капролактам представляет собой Белые кристаллы, хорошо растворимые в воде, спирте, эфире, бензоле. При нагревании в присутствии небольших количеств воды, спирта, аминов, органических кислот и некоторых других соединений капролактам полимеризуется с образованием полиамидной смолы, из которой получают волокно капрон. Важное свойство Капролактам - способность полимеризоваться с образованием ценного полимера - поликапроамида
Физические свойства капролактама
| Систематическое наименование | азепан-2-он |
| Традиционное название | капролактам |
| Описание | Белое, гигроскопичное, кристаллическое твердое вещество |
| Молекулярная формула | C6H11NO |
| Молярная масса | 113.16 г/моль |
| Плотность (при 70 °С) | 1,01 г/см3 |
| Точка кипения | 136-138 °C / 10 мм Hg |
| Точка плавления | 69-70 oC |
| Коэффициент перевода | 1ppm=4.6 мг/м3 @ 25 oC |
Основное промышленное применение капролактама - производство полиамидных (нилоновых) волокон и нитей (полиамид 6). Кроме того, капролактам применяется в производстве инженерных пластиков, полиамидных пленок
В небольших количествах капролактам может использоваться в образовании полиуретана и синтезе лизина, жесткие текстильные подкладки, покрытия для пленок, синтетические кожи, пластификаторы, растворители для красок.
Технология производства капролактама
В промышленности капролактам получают из бензола, фенола или толуола по схемам:
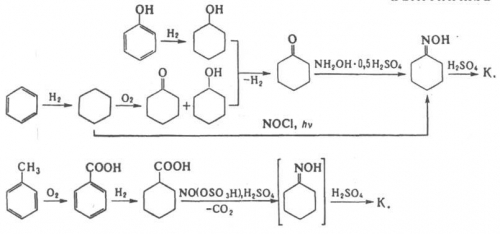
В промышленности наибольшее распространение получил метод синтеза капролактама из бензола. Технологическая схема включает гидрирование бензола в циклогексан в присутствии Pt/Al2O3 или никель-хромового катализатора при 250-350 и 130-220 °С, соответственно. Жидкофазное окисление циклогексана в циклогексанон осуществляют при 140-160°С, 0,9-1,1 МПа в присутствии нафтената или стеарата Со. Получающийся в результате окисления циклогексанол превращают в циклогексанон путем дегидрирования на цинк-хромовых (360-400 °С), цинк-железных (400 °С) или медь-магниевых (260-300 °С) смешанных катализаторах. Превращение в оксим проводят действием избытка водного раствора сульфата гидроксиламина в присутствии щелочи или NH3 при 0-100°С. Завершающая стадия синтеза капролактама. - обработка циклогексаноноксима олеумом или конц. H2SO4 при 60-120 °С (перегруппировка Бекмана). Выход капролактама в расчете на бензол 66-68%. При фотохимическом методе синтеза капролактама из бензола циклогексан подвергают фотохимическому нитрозированию в оксим под действием NOCl при УФ облучении. Метод синтеза капролактама из фенола включает гидрирование последнего в циклогексанол в газовой фазе над Pd/Al2O3 при 120-140°С, 1-1,5 МПа, дегидрирование полученного продукта в циклогексанон и дальнейшую обработку как в методе синтеза из бензола. Выход 86-88%.
Метод синтеза капролактама из толуола включает: окисление толуола при 165°С в присутствии бензоата Со; гидрирование получающейся бензойной кислоты при 170°С, 1,4-1,5 МПа в присутствии 5%-ной взвеси Pd на мелкодисперсном угле; нитрозирование циклогексанкарбоновой кислоты под действием нитрозилгидросульфата (нитрозилсерной к-ты) при 75 80 °С до капролактама-сырца. Некоторые стадии этой схемы недостаточно селективны, что приводит к необходимости сложной очистки получаемого капролактама. Выход капролактама 71% в расчете на исходный продукт.
Полученный любым из перечисленных методов капролактам предварительно очищают с помощью ионообменных смол, NaClO и КМnО4, а затем перегоняют. Побочный продукт производсства (NH4)2SO4 (2,5-5,2 т на 1 т К.), который используется в сельском хозяйстве в качестве минерального удобрения. Известны также методы получения капролактама из неароматического сырья (фурфурола, ацетилена, бутадиена, этиленоксида), которые не нашли промышленного применения.
Твердый капролактам транспортируют в бумажных пятислойных мешках с полиэтиленовым вкладышем, жидкий - в специально оборудованных цистернах с обогревом в атмосфере азота (содержание кислорода в азоте не должно превышать 0,0005%). Температура воспламенения - 135°С, т. самовоспламенения - 400 °С, нижний предел воспламенения 123°С; ЛД50 450 мг/м3 (мыши, вдыхание паров), ПДК 10 мг/м3.
В мире капролактам получают преимущественно из бензола - 83,6%, из фенола - 12%, из толуола - 4,4% К.
Отраслевая структура потребления
Всеобщая экономическая рецессия оказала значительное влияние на мировой рынок капролактама. Спрос на полиамидные волокна и пластики в текстильной и автомобильной отраслях в 2008 году упал, что в свою очередь повлекло снижение потребления капролактама. В 4 квартале 2008 года объемы продаж снизились в разных секторах до 40%. В целом по итогам 2008 года зафиксировано падение спроса на капролактам на 5-6%. В январе 2009 года спрос начал кое-как восстанавливаться во многом за счет накопленных производителями запасов за последний квартал прошлого года.
Динамика мирового спроса на капролактам, 1998-2008, тыс. тонн
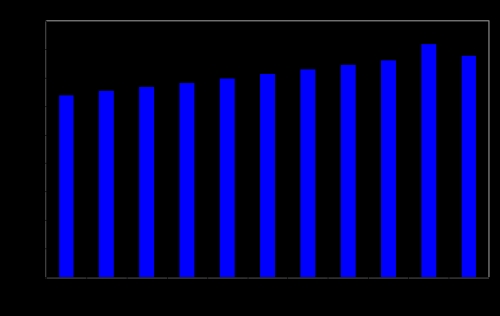
Источник: «SRI Consulting», «Yarns and Fibers Exchange»
Капролактам используется преимущественно в производстве полиамидных нитей и волокон, а также конструкционных пластиков. Около 60% мирового спроса приходится на нити и волокна, 34% - потребляется в производстве конструкционных пластмасс. Остальной объем используется для изготовления упаковочных пленок и других материалов.
Полиамидные волокна и нити, как правило, применяются в производстве текстиля, ковровых покрытий, промышленных нитей, используемых в свою очередь для изготовления шинного корда. Кордная нить – крупнейший и наиболее быстрорастущий сегмент рынка ПА6.
ПА6 смола также является основной для производства конструкционных пластиков, используемых для производства компонентов электронной и электрической техники, автомобильных деталей. В упаковочной отрасли применяется ориентированная полиамидная пленка, также изготовленная на основе ПА6. Небольшие объемы капролактама уходят на синтез лизина, а также в качестве агента в производстве полиуретана.
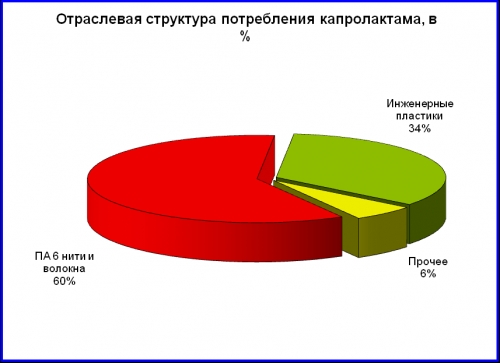
Источник: по данным ICB
С анализом российского и мирового рынков капролактама Вы можете познакомиться в отчете Академии Конъюнктуры Промышленных Рынков «Мировой рынок капролактама».