Это относится как к реакции разложения N2O [80], так и к реакции окисления бензола в фенол [60]. По отношению к последней реакции такой эффект хорошо виден из рис. 2, на котором приведена зависимость конверсии бензола от концентрации α-центров. Активность всех исследованных образцов описывается единой зависимостью и определяется только концентрацией α-центров. 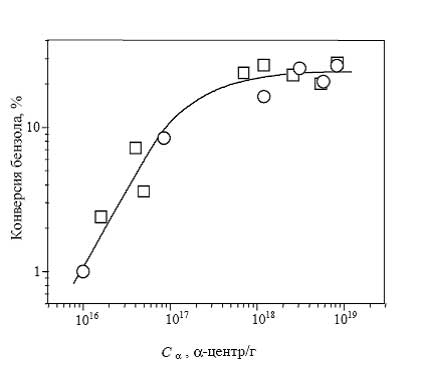
Рис. 2. Зависимость конверсии бензола от концентрации α-центров на цеолитах ZSM-5 состава Fe-Si (!) иFe-Al-Si (") при 350 °С Согласно квантовохимическим расчетам [81], α-центры представляют собой биядерные комплексы железа, которые формируются на стадии выхода Fe из кристаллической решетки цеолита при его термических обработках. Аналогично внерешеточному алюминию, эти комплексы являются координационно -ненасыщенными частицами и обладают льюисовской кислотностью. Учитывая сходный механизм образования внерешеточных частиц Fe и Al, естественно ожидать некоторую корреляцию между каталитической активностью и льюисовской кислотностью, что и наблюдали при различных высокотемпературных обработках одного и того же образца цеолита. Однако в случае образцов с различным химическим составом такая корреляция не должна существовать, что действительно и подтверждается [79]. Это объясняется тем, что в разных образцах неодинакова концентрация внерешеточных атомов Al, которые дают основной вклад в льюисовскую кислотность, но не дают вклада в каталитическую активность. Квантовохимические расчеты также не подтверждают каталитическую роль льюисовских центров [82].Каталитическая активность железа в реакциях окисления закисью азота подтверждена в ряде работ других авторов [69, 70, 83]. Интересно, что образование α-центров приводит к качественному изменению в состоянии железа по сравнению с атомами Fe на поверхности оксида Fe2O3. В составе α-центров атомы Fe теряют способность активировать молекулярный кислород, но приобретают повышенную способность к активации молекул N2O [80]. Это ярко проявляется в реакции окисления бензола с помощью этих молекул (табл. 2). Так, в присутствии закиси азота конверсия бензола составляет 27% при 350 оС, тогда как в присутствии О2 - только 0,3% при 500 оС. Более того, при этом изменяется направление реакции: если при действии N2O с высокой селективностью образуется фенол, то в случае О2 регистрируются лишь продукты полного окисления. На оксиде железа ни один из окислителей не приводит к образованию фенола. ГЕННАДИЙ ИВАНОВИЧ ПАНОВ - доктор химических наук, заведующий лабораторией окислительного катализа на цеолитах Института катализа им. Г. К. Борескова СО РАН. Область научных интересов: окислительный катализ, механизм каталитических реакций. АЛЕКСАНДР СЕРГЕЕВИЧ ХАРИТОНОВ - доктор химических наук, ведущий научный сотрудник Института катализа им. Г. К. Борескова СО РАН. Область научных интересов: каталитическое окисление органических соединений, цеолиты, технология каталитических процессов. 630090 Новосибирск, просп. акад. Лаврентьева, 5, Институт катализа СО РАН, тел. (3832)34-44-52, факс (3832)34-30-56, E-mail Panov@catalysis.nsk.su, Khar@catalysis.nsk.su Подробнее с текущей ситуацией и прогнозом развития российского рынка фенола и ацетона можно познакомиться в отчете Академии Конъюнктуры Промышленных Рынков «Рынок фенола и ацетона в России». | 